La cura antibiotica rappresenta uno strumento terapeutico fondamentale nella lotta contro le infezioni batteriche, ma la sua azione non è priva di conseguenze per l'organismo. Infatti, oltre a colpire i batteri patogeni, gli antibiotici possono danneggiare anche la preziosa flora batterica intestinale, un ecosistema complesso e vitale per il nostro benessere generale. È qui che entrano in gioco i probiotici, microrganismi vivi che, se assunti in quantità adeguate, offrono un beneficio alla salute dell'ospite, principalmente riequilibrando la flora intestinale alterata.
Gli antibiotici sono farmaci essenziali nella medicina moderna, progettati specificamente per combattere le infezioni causate dai batteri. La loro efficacia è strettamente legata al tipo di batterio che provoca l'infezione, rendendo cruciale la prescrizione medica basata, quando possibile, sull'identificazione del patogeno responsabile tramite test specifici.
Abbiamo detto che gli antibiotici sono potenti armi contro i batteri patogeni. Purtroppo, questa azione non è sempre chirurgica: gli antibiotici non distinguono facilmente tra batteri "cattivi" che causano l'infezione e batteri "buoni" che popolano il nostro corpo, in particolare l'intestino. Quando si assume un antibiotico, si verifica un'alterazione di questo delicato ecosistema, nota come disbiosi intestinale. La disbiosi intestinale è una condizione di squilibrio nel microbiota. Durante e dopo una terapia antibiotica, la disbiosi è una conseguenza frequente.
L'effetto più immediato e riconoscibile della disbiosi indotta dagli antibiotici è a livello gastrointestinale. La diarrea associata all'uso di antibiotici colpisce una percentuale significativa di pazienti, variabile a seconda del tipo di antibiotico, della dose e della durata del trattamento.
I probiotici sono definiti dall'Organizzazione Mondiale della Sanità (OMS) come "microrganismi vivi che, se somministrati in quantità adeguate, conferiscono un beneficio alla salute dell'ospite". Non tutti i microrganismi sono probiotici. È fondamentale capire che i benefici dei probiotici sono specifici del ceppo. Ciò significa che un beneficio dimostrato per un particolare ceppo di Lactobacillus acidophilus non si applica necessariamente a un altro ceppo della stessa specie o a un'altra specie di Lactobacillus.
La ragione principale per abbinare probiotici e antibiotici è chiara: contrastare gli effetti negativi degli antibiotici sull'intestino e preservare o ripristinare l'equilibrio della flora batterica. Prendere probiotici con antibiotici è raccomandato principalmente per contrastare gli effetti negativi degli antibiotici sulla flora intestinale, in particolare per prevenire o ridurre l'incidenza e la severità della diarrea associata all'uso di antibiotici (AAD). Molti studi hanno dimostrato che l'uso concomitante di probiotici con antibiotici può ridurre significativamente il rischio di sviluppare AAD.
Anche se non si manifesta la diarrea, l'intestino subisce comunque lo stress della terapia antibiotica. L'assunzione di probiotici può aiutare a mitigare altri sintomi della disbiosi, come gonfiore e dolori, e a supportare una più rapida ripresa delle normali funzioni intestinali dopo la fine del trattamento. Un intestino sano e un microbiota equilibrato sono fondamentali per un sistema immunitario efficiente. Supportando la salute intestinale, i probiotici possono indirettamente aiutare l'organismo a combattere meglio le infezioni.
Antibiotici vs Probiotici: Meccanismi d'Azione a Confronto
Antibiotici e probiotici agiscono entrambi sul microbiota intestinale, ma con effetti contrapposti. Hanno il nome molto simile e in qualche modo entrambi hanno a che fare con i batteri e con il microbiota. Ma antibiotici e probiotici non sono affatto la stessa cosa, anzi. Le differenze tra antibiotico e probiotico sono profonde. Gli antibiotici sono farmaci che si assumono per eliminare, in maniera più o meno selettiva, i batteri patogeni.
Il target d’azione degli antibiotici sono i batteri: questi farmaci vengono infatti somministrati con lo scopo di bloccarne la replicazione (antibiotici batteriostatici), dando modo al sistema immunitario di combattere l’infezione, o provocarne la morte (battericidi). Ecco perché gli antibiotici devono essere assunti, sotto controllo medico, solo in caso di infezioni batteriche (possibilmente accertate con esami specifici, come per esempio tamponi faringei o un’urinocoltura con antibiogramma nel caso, rispettivamente, del sospetto di una faringite batterica o di un’infezione delle vie urinarie) e non in occasione di sindromi influenzali che, in generale, sono veicolate da virus.
Essendo diversi gli attori in gioco (batteri in un caso, virus nell’altro), gli antibiotici sono infatti del tutto inutili in caso di influenza, indipendentemente dai sintomi che provoca (intestinali o respiratori). Anzi, il loro uso inappropriato causa un aumento del rischio di antibiotico-resistenza, ovvero lo sviluppo di batteri in grado di resistere agli antibiotici attualmente in uso. Il vero pericolo è che i batteri diventino resistenti alla penicillina e una volta che questa resistenza si sviluppa, perdura per molto tempo. Un impiego errato di antibiotici porta i batteri a “imparare” a difendersi da essi: i batteri che sopravvivono al contatto con il farmaco sviluppano antibiotico resistenza e trasmettono questa capacità alle generazioni future, rendendo inefficace il principio attivo alla successiva somministrazione.
Particolarmente problematico è l’uso ravvicinato di diversi antibiotici, che favorisce la comparsa di ceppi resistenti in grado di proliferare nel corpo e causare gravi malattie. Questi batteri multiresistenti possono essere trasmessi direttamente o indirettamente tra persone, tra esseri umani e animali, e anche attraverso l’ambiente. Il rischio di infezione è particolarmente alto in contesti con persone fragili o malate, come ospedali e case di riposo.
Nonostante ciò, gli antibiotici restano imprescindibili nella medicina moderna: grazie a questa scoperta avvenuta oltre 90 anni fa, infezioni un tempo potenzialmente letali possono oggi essere curate. Tuttavia, i rischi legati all’antibiotico resistenza e agli effetti collaterali sono stati a lungo sottovalutati.
Invece, i probiotici sono microrganismi vivi che, se somministrati in quantità adeguate, conferiscono un beneficio alla salute dell’ospite. Il loro ruolo è quello di ripristinare e mantenere l'equilibrio della flora batterica intestinale, contrastando la proliferazione di batteri patogeni e supportando le funzioni immunitarie.

La Disbiosi Intestinale: Una Conseguenza Comune della Terapia Antibiotica
Uno degli effetti collaterali delle terapie antibiotiche è la disbiosi, ovvero l’alterazione della composizione della flora (o microbiota) intestinale. Per ripristinare il giusto equilibrio ed evitare effetti collaterali associati all’assunzione di antibiotici, come la diarrea, non è sufficiente, come alcuni pensano, mangiare yogurt.
L’alterazione dell’equilibrio tra microrganismi benefici e patogeni è conosciuta come disbiosi intestinale. Questa condizione dà luogo a una serie di sintomi relativi al tratto gastrointestinale. Capita a tutti di dover prendere gli antibiotici ma spesso possono avere effetti collaterali sull'equilibrio intestinale, causando disturbi come diarrea, gonfiore e senso di pesantezza.
La diarrea da antibiotico (dall’inglese AAD) è infatti un effetto collaterale comune che coinvolge fino al 25% dei pazienti. Questo si verifica perché gli antibiotici non distinguono tra batteri benefici e agenti patogeni e provocano un forte squilibrio nel nostro microbiota intestinale. L’AAD viene diagnosticata quando la diarrea compare durante o subito dopo una terapia antibiotica e altre cause della diarrea possono essere escluse. La diarrea da antibiotico può manifestarsi settimane dopo la sospensione del farmaco, motivo per cui non viene sempre associata all’antibiotico.
Tra le cause più frequenti c’è il batterio Clostridium difficile, responsabile di circa il 25% dei casi di diarrea associata agli antibiotici. A causa della drastica riduzione della flora intestinale “buona”, i patogeni hanno vita facile: possono insediarsi e moltiplicarsi nel nostro intestino indisturbati senza quasi incontrare resistenza da parte delle nostre difese naturali. Questo scenario può dare origine a infiammazioni del tratto intestinale, causate dalle tossine prodotte dai batteri stessi.
Quando l’equilibrio dell’intestino si altera, si indebolisce anche il suo strato di difesa più importante: il muco che ricopre la mucosa intestinale. Questo strato funziona come una vera e propria barriera che protegge la parete dell’intestino da sostanze irritanti, batteri dannosi e infiammazioni. Per questo motivo, la produzione sufficiente di muco protettivo è indispensabile la presenza della flora intestinale “buona”. Questi batteri benefici producono una sostanza chiamata butirrato, un acido grasso che rappresenta la principale fonte di energia per le cellule della mucosa intestinale, in particolare per le cellule caliciformi, che sono quelle incaricate di produrre il muco. Se queste cellule non ricevono abbastanza energia - ad esempio perché la flora batterica è impoverita o alterata - riescono a produrre meno muco. Di conseguenza, lo strato protettivo si assottiglia e la parete dell’intestino rimane meno difesa e molto più vulnerabile a irritazioni e infiammazioni.
La riduzione della flora intestinale causata dagli antibiotici non è quasi mai temporanea. È noto da tempo che gli antibiotici abbiano un effetto drastico sulla biodiversità del microbioma - la cosiddetta diversità - e che il microbiota intestinale fatichi a rigenerarsi spontaneamente dopo una terapia antibiotica. Ogni ceppo batterico svolge una funzione specifica nell’intestino: quando viene a mancare, alcuni batteri patogeni possono proliferare più facilmente.
Inoltre, l’assorbimento di nutrienti essenziali e sostanze vitali può risultare compromesso. Questo può portare a una produzione insufficiente di ormoni come la serotonina e innescare una serie di reazioni a catena. Sebbene una corretta alimentazione e uno stile di vita possano aiutare il recupero parziale della flora intestinale, spesso nel microbiota rimangono comunque degli squilibri.
Quando e Come Assumere i Probiotici Durante una Terapia Antibiotica
Abbinare probiotici e antibiotici richiede attenzione, soprattutto per quanto riguarda i tempi di assunzione e la scelta del prodotto. È fondamentale assumere i probiotici a distanza di almeno 2-3 ore dall'antibiotico. Questo intervallo di tempo è cruciale perché permette ai probiotici di passare attraverso il tratto gastrointestinale senza essere immediatamente inattivati dalla concentrazione di antibiotico presente nell'intestino in quel momento, massimizzando così la loro sopravvivenza e capacità di colonizzazione temporanea. Ad esempio, se prendi l'antibiotico alle 8:00 del mattino, puoi prendere il probiotico non prima delle 10:00 o delle 11:00.
La terapia probiotica non dovrebbe limitarsi solo alla durata della cura antibiotica, ma è consigliabile continuarla per un periodo successivo, che può variare da almeno una a quattro settimane (o anche più, a seconda del caso specifico e del consiglio del professionista sanitario). La durata esatta può dipendere dalla durata della terapia antibiotica, dalla gravità dell'alterazione intestinale percepita (es. se c'è stata diarrea) e dalle specifiche caratteristiche del probiotico utilizzato.
Il dosaggio dei probiotici si misura in Unità Formanti Colonia (UFC). Per la gestione degli effetti degli antibiotici, le dosi efficaci negli studi si aggirano solitamente nell'ordine di diversi miliardi di UFC al giorno.

La Scelta del Probiotico Giusto: Criteri e Raccomandazioni
Come accennato, l'efficacia dei probiotici è ceppo-specifica. Per la prevenzione o il trattamento della diarrea associata all'uso di antibiotici (AAD), alcuni ceppi hanno mostrato maggiore efficacia nei trial clinici. Miscele contenenti specifici ceppi di Lactobacillus (come L. acidophilus, L. casei) e Bifidobacterium (come B. lactis, B. animalis) sono spesso raccomandate.
È consigliabile scegliere prodotti che indichino chiaramente sulla confezione i ceppi batterici contenuti (nome scientifico completo: genere, specie e sigla del ceppo) e il numero di unità formanti colonia (UFC), che indica la quantità di microrganismi vivi. Considera anche la forma farmaceutica: capsule, bustine, flaconcini.
Molti fermenti lattici non superano l’acidità gastrica, non arrivano vivi al colon, o non sono in grado di instaurare interazioni utili con la flora intestinale. Al contrario, la definizione di probiotico è recente e rigorosa. Anche quando si parla di probiotici, la normativa richiede di dichiarare il numero di microrganismi vivi presenti nella dose giornaliera, espresso in Unità Formanti Colonia (UFC) e garantito fino al termine della shelf-life del prodotto. È un requisito fondamentale per assicurare che il probiotico possa raggiungere l’intestino vitale e in quantità efficace, come previsto dalla sua stessa definizione scientifica.
L'utilizzo del termine “fermenti” in questa dicitura tecnica non rimanda ai fermenti lattici generici, ma alla modalità con cui si quantifica la vitalità dei microrganismi. In Europa, le affermazioni salutistiche sono regolamentate in modo stringente. Dove agiscono davvero? Il microbiota non è distribuito in modo uniforme. È nel colon che si concentra la maggior parte dei microrganismi intestinali, in un ecosistema dominato - nell’infanzia - dai bifidobatteri. Questi batteri svolgono funzioni chiave nella digestione, nella barriera intestinale e nell’immunità. Tuttavia, sono anche tra i più vulnerabili all’azione degli antibiotici.
Una survey condotta su 279 pediatri italiani mostra che il 63% prescrive abitualmente un probiotico durante la terapia antibiotica, con l’obiettivo di ridurre disturbi gastrointestinali e sostenere l’eubiosi nei piccoli pazienti. La scelta dei ceppi, però, non può essere casuale. Se un probiotico non sopravvive alla molecola antibiotica associata, non può esercitare un reale effetto protettivo nel momento in cui servirebbe di più. Quando si affronta un trattamento antibiotico, l’attenzione è naturalmente rivolta all’infezione da curare. Ma è altrettanto importante considerare gli effetti collaterali sul microbiota, soprattutto nei bambini, in cui i bifidobatteri rappresentano una difesa fisiologica fondamentale. Distinguere tra fermenti lattici e probiotici significa riconoscere quali microrganismi sono in grado di sostenere concretamente il benessere intestinale.
Probiotici e Popolazioni Vulnerabili: Bambini e Anziani
I bambini sono frequentemente soggetti a terapie antibiotiche, e il loro microbiota intestinale è ancora in fase di sviluppo o può essere più suscettibile alle alterazioni. L'uso di probiotici (in particolare Lactobacillus rhamnosus GG e Saccharomyces boulardii, che sono tra i più studiati e validati per l'età pediatrica) è ampiamente raccomandato dai pediatri per prevenire o ridurre l'AAD nei bambini che assumono antibiotici. È fondamentale scegliere formulazioni specifiche per l'età pediatrica (come gocce, bustine predosate) e seguire scrupolosamente le indicazioni del pediatra o del farmacista riguardo al dosaggio e alla durata.
Gli anziani possono avere un microbiota intestinale già alterato a causa dell'età, di patologie concomitanti o dell'uso di altri farmaci. L'integrazione con probiotici può essere particolarmente benefica negli anziani in terapia antibiotica per aiutare a sostenere la resilienza del microbiota e ridurre il rischio di complicazioni intestinali. Anche in questo caso, ceppi come Lactobacillus rhamnosus GG e Saccharomyces boulardii, o miscele multiceppo mirate, possono essere scelte appropriate.
Gruppi di persone vulnerabili, come gli anziani nelle case di riposo, possono trarre particolare beneficio dall’assunzione di probiotici, in concomitanza di una terapia antibiotica. In questi contesti, l’impiego di probiotici adeguati può rivelarsi particolarmente utile: la diarrea da antibiotico può infatti comportare complicazioni come una marcata disidratazione e, di conseguenza, la necessità di ricovero ospedaliero. In media, circa il 10% dei residenti nelle case di riposo riceve regolarmente antibiotici, spesso per trattare infezioni urinarie, infezioni respiratorie basse o infezioni cutanee. L’incidenza della diarrea associata ad antibiotici può arrivare fino al 25%, a seconda del tipo di antibiotico utilizzato.
Probiotici e antibiotici: è sempre sbagliato usarli insieme?
Errori Comuni e Rimedi Naturali
Assumere probiotici contemporaneamente agli antibiotici: Questo è l'errore più frequente. Interrompere l'assunzione dei probiotici troppo presto: Smettere di prendere i probiotici appena finisce la cura antibiotica riduce la loro capacità di supportare il ripristino completo del microbiota. Usare probiotici generici senza ceppi specifici: Non tutti i probiotici sono efficaci per l'AAD. Non considerare la qualità del prodotto: La vitalità dei microrganismi nel prodotto è fondamentale.
Prebiotici: I prebiotici sono fibre non digeribili che fungono da "cibo" per i batteri benefici già presenti nell'intestino (sia quelli endogeni che i probiotici assunti). Alimenti ricchi di prebiotici includono aglio, cipolla, porri, asparagi, banane, cicoria, topinambur, legumi, avena.
Alimentazione: Seguire una dieta equilibrata e ricca di fibre è sempre importante per la salute intestinale. Durante e dopo una cura antibiotica, privilegiare alimenti facilmente digeribili ma ricchi di nutrienti. Consumare cibi fermentati naturalmente ricchi di batteri benefici (come yogurt con colture vive, kefir, crauti, kimchi - attenzione però che la quantità e la varietà di batteri in questi alimenti potrebbero non essere sufficienti o specifiche come quelle degli integratori probiotici per l'AAD). Evitare cibi eccessivamente grassi, zuccherati o trasformati che possono irritare ulteriormente l'intestino.
Per prima cosa, i cambiamenti osservati nel microbioma a seguito dell'utilizzo dei probiotici non devono spaventare. In una persona sana difficilmente possono avere conseguenze nocive, o quanto meno non ne hanno di gravi. Non si può escludere però che aumentino al suscettibilità ad alcune patologie del tratto intestinale, o che più in generale abbiano effetti di qualche tipo sulla salute. Per questo motivo, c'è chi ne sconsiglia l'assunzione, e raccomanda di ricorrere a rimedi più naturali: alimenti ricchi di fibre, capaci di attraversare intatte lo stomaco, e andare poi ad alimentare la fermentazione batterica nell'intestino. Con una dieta a base di frutta, verdura e prodotti integrali i batteri buoni del nostro intestino hanno maggiore facilità a resistere e riprendersi dopo un ciclo di antibiotici.
| Caratteristica | Antibiotici | Probiotici |
|---|---|---|
| Scopo Principale | Eliminare batteri patogeni | Ripristinare e mantenere l'equilibrio della flora intestinale |
| Meccanismo d'Azione | Battericida o batteriostatico | Competizione con patogeni, modulazione immunitaria, produzione di sostanze benefiche |
| Effetto sulla Flora | Può danneggiare la flora benefica (disbiosi) | Supporta e riequilibra la flora benefica |
| Utilizzo | Trattamento di infezioni batteriche | Prevenzione e gestione di disturbi gastrointestinali, supporto immunitario |
| Necessità di Prescrizione Medica | Sì | Generalmente no (ma consigliato il parere medico) |
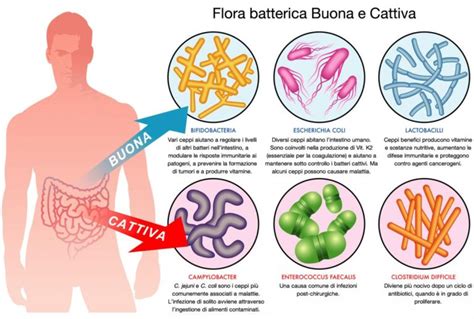
La microflora intestinale si inizia a formare a partire dalla nascita, tramite i germi del canale del parto; quindi, continua a svilupparsi fino all’età di tre anni, quando la sua composizione risulta pressoché stabile. La popolazione microbica può essere ripartita in base al comportamento dei batteri della flora intestinale verso l’ospite umano.
La terapia antibiotica è un salvavita, ma il suo impatto sulla flora intestinale è una realtà da non sottovalutare. Prendersi cura del proprio microbiota intestinale significa investire nel proprio benessere generale e nella resilienza del proprio organismo.
tags: #probiotici #sono #antibiotici