Le proteine che introduciamo con la nostra alimentazione subiscono un processo di idrolisi nello stomaco e nell'intestino tenue. Questo meccanismo biochimico trasforma le proteine in amminoacidi liberi e oligopeptidi, rendendoli disponibili per l'assorbimento e l'utilizzo da parte dell'organismo.
Il catabolismo degli amminoacidi, ovvero il loro processo di degradazione, inizia con l'allontanamento del gruppo amminico. Una volta rimosso questo gruppo, lo scheletro carbonioso rimanente viene indirizzato verso importanti vie metaboliche. Può essere utilizzato nel ciclo di Krebs, un processo centrale per la produzione di energia cellulare, oppure nella gluconeogenesi, la via biosintetica che porta alla formazione di glucosio.
Ruolo delle Transaminasi nel Metabolismo degli Amminoacidi
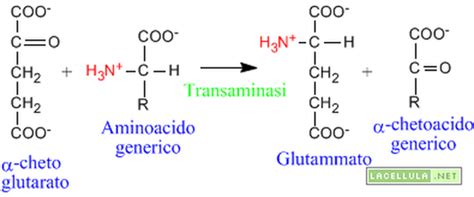
Le amminotransferasi, comunemente note come transaminasi, svolgono un ruolo cruciale nella rimozione del gruppo amminico dagli amminoacidi. Queste reazioni, definite transaminazioni, implicano il trasferimento di un gruppo amminico da un amminoacido donatore all'alfa-chetoglutarato. Come risultato di questa reazione, si forma il glutammato, un amminoacido che funge da importante collettore di gruppi amminici. Contemporaneamente, il gruppo amminico del donatore viene convertito nel corrispondente α-chetoacido.
Il glutammato, una volta formato, ha due destini principali: può convogliare i gruppi amminici verso il ciclo dell'urea, il processo deputato alla detossificazione dell'ammoniaca, oppure può partecipare alle vie biosintetiche per la sintesi di altri amminoacidi. Il coenzima indispensabile per l'attività delle transaminasi è il piridossalfosfato, una forma attiva della piridossina, nota anche come Vitamina B6.
Una caratteristica fondamentale delle reazioni di transaminazione è la loro reversibilità. Ciò significa che possono funzionare in entrambi i sensi, adattandosi alle specifiche necessità metaboliche della cellula in un dato momento. Generalmente, i gruppi amminici in eccesso vengono escreti dall'organismo o utilizzati per la sintesi di altre molecole contenenti azoto.
Deamminazione Ossidativa e Trasporto dell'Ammoniaca
Un altro processo fondamentale a cui vanno incontro gli amminoacidi è la deamminazione ossidativa. Questa reazione avviene all'interno dei mitocondri ed è catalizzata da un enzima chiave: la glutammato deidrogenasi. Questo enzima rimuove il gruppo amminico dal glutammato, sostituendolo con un atomo di ossigeno proveniente dall'acqua. Durante questo processo si libera ione ammonio (NH4+).
Lo ione ammonio, altamente tossico per le cellule, viene immediatamente neutralizzato. Una delle vie di neutralizzazione prevede la reazione con il glutammato, catalizzata dall'enzima glutammina sintetasi in una reazione che richiede ATP. Questa reazione forma la glutammina, un amminoacido che agisce come trasportatore di gruppi amminici, in particolare verso il fegato. La glutammina, una volta entrata nel circolo sanguigno, raggiunge il fegato. Qui, all'interno dei mitocondri epatici, la glutammina viene riconvertita a glutammato, con il rilascio dello ione ammonio (NH4+).
Un altro importante trasportatore di gruppi amminici, specialmente dal tessuto muscolare al fegato, è l'alanina. L'alanina viene sintetizzata attraverso il trasferimento del gruppo amminico dal glutammato all'acido piruvico (piruvato). Una volta giunta nel fegato e all'interno dei mitocondri epatici, l'alanina rilascia il proprio ione ammonio, rigenerando glutammato e piruvato. Il piruvato è una molecola essenziale per il fegato, poiché viene utilizzato nel processo di gluconeogenesi.
Il Ciclo dell'Urea e la Detossificazione dell'Ammoniaca
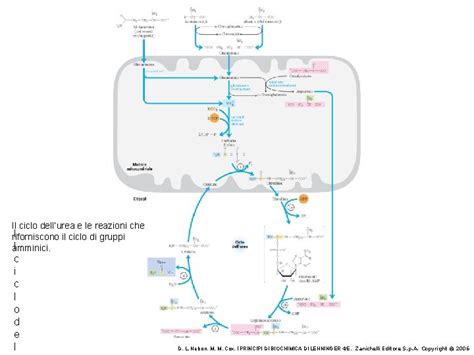
Lo ione ammonio (NH4+) è estremamente tossico per l'organismo, in particolare per il cervello. Come abbiamo visto, al di fuori del fegato (in sede extraepatica), lo ione ammonio viene neutralizzato legandosi al glutammato o al piruvato. Nel fegato, tuttavia, l'NH4+ viene incorporato in una molecola non tossica: l'urea. Questo processo avviene attraverso il ciclo dell'urea.
Il ciclo dell'urea inizia con la formazione del carbamil fosfato, una reazione catalizzata dall'enzima carbamil-fosfato sintetasi. Questa fase iniziale del ciclo richiede un notevole dispendio energetico, consumando due molecole di ATP. Le successive reazioni del ciclo portano alla formazione finale dell'urea. È importante sottolineare che l'intero ciclo dell'urea è un processo che richiede una quantità significativa di energia, con un consumo totale di 4 molecole di ATP per ogni molecola di urea prodotta.
Ciclo dell'Urea
Destino degli Scheletri Carboniosi degli Amminoacidi
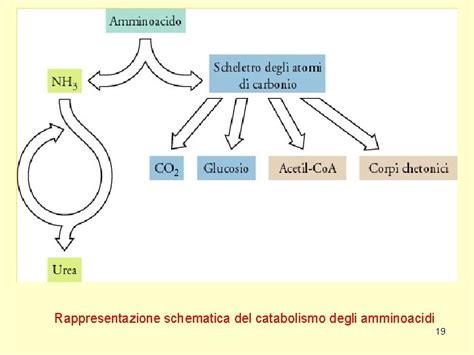
Oltre alla gestione dei gruppi amminici, il destino degli scheletri carboniosi degli amminoacidi è altrettanto significativo dal punto di vista metabolico. Questi scheletri vengono principalmente indirizzati verso il ciclo di Krebs, dove contribuiscono alla produzione di energia. Come illustrato in figura, gli scheletri carboniosi degli amminoacidi convergono in sette composti chiave che possono entrare direttamente o indirettamente nel ciclo di Krebs: piruvato, acetil-CoA, acetoacetil-CoA, α-chetoglutarato, succinil-CoA, fumarato e ossalacetato.
Gli amminoacidi che vengono degradati ad acetil-CoA o acetoacetil-CoA sono definiti "chetogenetici". Questo perché possono essere precursori per la sintesi dei corpi chetonici, molecole energetiche alternative al glucosio. Gli altri amminoacidi, invece, sono definiti "glucogenetici". Essi, una volta convertiti in piruvato e ossalacetato, possono essere utilizzati dal fegato per formare glucosio attraverso il processo di gluconeogenesi, contribuendo così a mantenere stabili i livelli di glicemia.
| Amminoacidi Chetogenetici | Amminoacidi Glucogenetici | Amminoacidi Sia Chetogenetici che Glucogenetici |
|---|---|---|
| Leucina, Lisina | Alanina, Arginina, Asparagina, Aspartato, Cisteina, Acido aspartico, Glutammato, Glutammina, Glicina, Istidina, Metionina, Prolina, Serina, Treonina, Triptofano, Tirosina, Valina | Isoleucina, Fenilalanina, Triptofano, Tirosina |
tags: #intercalazione #aminoacidi #in #idrotalcite