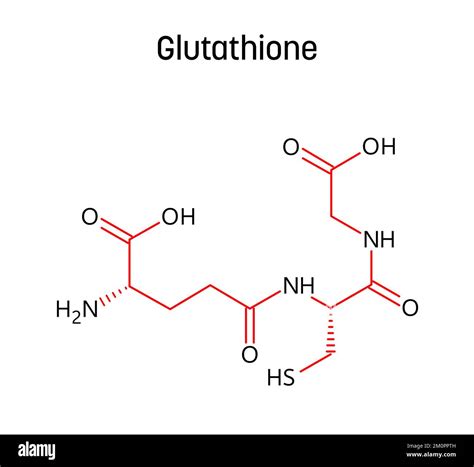
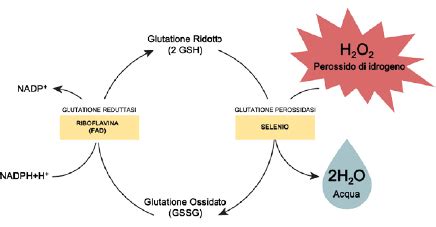
Il glutatione (GSH) è la principale molecola tiolica non proteica presente nelle cellule animali. Nel citoplasma, viene sintetizzata da cisteina, acido glutammico e glicina, attraverso reazioni biochimiche dipendenti dall'adenosina trifosfato (ATP). Il mantenimento dell'equilibrio redox intracellulare avviene tramite un ciclo: la glutatione perossidasi ossida il GSH a glutatione disolfuro (GSSG), e il GSSG viene poi ridotto dalla glutatione reduttasi, ritornando a GSH. Mantenere l'equilibrio del rapporto GSH/GSSG è fondamentale per controllare la crescita, lo sviluppo e la difesa ossidativa delle cellule; pertanto, il loro rapporto è un indicatore di salute cellulare. Il GSSG deve essere in massima parte riconvertito in GSH, la forma ridotta che contrasta i ROS e svolge altri importanti compiti.
Le concentrazioni di GSH totale sono fisiologicamente basse nel plasma (1-6 μM), ma molto più alte nelle cellule (1-10 mM), comprese le componenti del sangue come gli eritrociti. Il GSH ha un ruolo molto importante in numerose vie metaboliche, tra cui la sintesi del DNA e delle proteine, il trasporto degli aminoacidi, le attivazioni enzimatiche, il funzionamento del sistema immunitario, la rimozione dei radicali liberi, il trasferimento degli aminoacidi attraverso le membrane cellulari e la disintossicazione dagli xenobiotici (come farmaci e inquinanti). Inoltre, è essenziale per il mantenimento dei gruppi solfidrici delle proteine, del DNA dei mitocondri e per il loro corretto funzionamento.
I ROS (specie reattive dell'ossigeno) entro certi livelli sono coinvolti in vari sistemi di segnalazione molecolare, essendo quindi necessari all'omeostasi mitocondriale e cellulare. Per mantenere questo equilibrio, i mitocondri necessitano di una costante protezione dall'eccesso di ROS, esercitata dai sistemi antiossidanti cellulari. Tra questi, il GSH, e in particolare il glutatione mitocondriale (mGSH), svolge un ruolo chiave nei mitocondri. Trasportato dal citoplasma tramite proteine trasportatrici (carriers), il mGSH svolge attività antiossidante e disintossicante, stabilizza il DNA mitocondriale ed è coinvolto in altri meccanismi come la fosforilazione ossidativa (OXPHOS) per la produzione di ATP e la biosintesi delle proteine ferro-zolfo.
Il mGSH rappresenta il 10-15% del GSH cellulare. In condizioni fisiologiche, l'85% del GSH si trova nella forma ridotta nel citoplasma, mentre nei mitocondri il GSH è presente in concentrazioni superiori (circa 99%) a causa del ridotto volume della matrice mitocondriale, con il GSSG inferiore all'1%. In caso di eccesso di ROS, si assiste all'abbassamento delle concentrazioni fisiologiche di mGSH, con conseguente riduzione significativa della respirazione mitocondriale basale e della produzione di ATP. La carenza di GSH è considerata un segno distintivo di alterazione delle attività mitocondriali. Quando l'eccesso di ROS non viene più adeguatamente neutralizzato, si instaura la disfunzione mitocondriale, che prelude alla morte cellulare programmata (apoptosi, autofagia, necroptosi, ferroptosi).
Oltre al GSH, l'azione antiossidante è svolta anche da altre molecole fisiologicamente presenti nelle cellule e nei mitocondri, attraverso il sistema antiossidante enzimatico e quello non enzimatico. Stimolare la sintesi di GSH contribuisce a prevenire la perdita di potenziale di membrana mitocondriale e inibire l'apoptosi.
Glutatione a livello cutaneo e sistemico
A livello cutaneo, antiossidanti come il GSH, la vitamina C ed E, il coenzima Q10, la catalasi (CAT) e la superossido dismutasi (SOD) sono concentrati negli strati più profondi dell'epidermide. Questa distribuzione protegge le cellule staminali epidermiche presenti nella giunzione derma-epidermica, dove avviene la maggiore produzione di ROS. Fattori ambientali come i raggi UV e gli inquinanti atmosferici stimolano la produzione di ROS, comportando un maggiore consumo del GSH cellulare. Con l'avanzare dell'età, oltre all'aumento dei ROS, diminuisce la capacità di sintesi e riciclaggio del GSH, alterando il rapporto GSH/GSSG. Ciò comporta una diminuzione delle difese antiossidanti e disintossicanti a livello cutaneo, accelerando l'insorgenza dei segni dell'invecchiamento, fenomeno riscontrabile anche nei follicoli piliferi.
A livello sistemico, la ridotta disponibilità di GSH cellulare, come di altri antiossidanti, è associata a molte condizioni patologiche caratterizzate da aumento dello stress ossidativo, processi infiammatori e disfunzione mitocondriale. Studi hanno confermato l'associazione tra bassi livelli di GSH e un alto tasso di multimorbilità in soggetti anziani. Bassi livelli di GSH e un basso rapporto GSH/GSSG sono presenti nelle malattie cardiometaboliche, respiratorie croniche (asma, BPCO), epatopatie e nei fumatori. Anche l'insorgenza delle malattie di Alzheimer e Parkinson è in parte associata al declino del GSH, contribuendo ad esacerbare lo stress ossidativo e generando neuroinfiammazione.
Una revisione sistematica ha confermato il declino dei livelli di GSH nel corso della vita adulta, evidenziando l'incremento dello stress ossidativo a carico delle strutture cerebrali. La valutazione dei livelli di GSH viene prospettata come ulteriore parametro per stimare l'età biologica. Ridotti livelli di GSH sono stati osservati negli stati infiammatori causati da infezioni microbiche e virali. Esistono anche differenze di genere, con livelli superiori nelle donne rispetto agli uomini. Un recente studio ha individuato nel basso apporto proteico negli anziani una delle cause della ridotta sintesi di GSH.
Come mantenere/ripristinare adeguati livelli intracellulari di GSH
Contrastare il declino del GSH rappresenta un importante obiettivo nei trattamenti contro i meccanismi molecolari, cellulari e tissutali che determinano l'invecchiamento sistemico e cutaneo. La somministrazione orale di GSH presenta criticità legate alla bassa biodisponibilità, poiché viene scomposto negli aminoacidi che lo costituiscono nel tratto gastro-intestinale, e alla ridotta penetrazione nelle cellule. Sebbene siano state studiate nuove formulazioni orali con promettenti risultati preliminari, la via parenterale per l'uso clinico, oltre alla via intra-nasale e sublinguale, risultano problematiche o inefficaci.
L'uso dei precursori di GSH nasce dalla constatazione che la disponibilità di cisteina è il fattore limitante per la sintesi di GSH. Il precursore di cisteina maggiormente studiato ed utilizzato in clinica è la N-acetilcisteina (NAC). Per via orale, la NAC viene rapidamente assorbita nell'intestino tenue, raggiunge il picco di concentrazione plasmatica tra 30 minuti e un'ora, per poi essere sottoposta a metabolismo epatico. I meccanismi di rilascio di H2S contribuiscono a inibire l'apoptosi, migliorare la bioenergetica mitocondriale e svolgere funzioni antiossidanti. Il rilascio di cisteina da parte della NAC produce ulteriori derivati solforati con importanti effetti protettivi sulle cellule, aggiuntivi a quelli derivanti dalla sintesi di GSH. La NAC possiede anche capacità antinfiammatorie, riducendo la produzione di citochine.
Da molti anni la NAC viene utilizzata per via infusionale come antidoto nel sovradosaggio di paracetamolo, oltre alla somministrazione orale come mucolitico. Esiste una vasta documentazione scientifica sull'uso clinico della NAC in ambito cardiovascolare, pneumologico, dermatologico e neuro-psichiatrico. In ottica antiaging, la NAC contribuisce a contrastare lo stress ossidativo provocato dai raggi UV, causa del foto-invecchiamento, e interviene nei meccanismi infiammatori cutanei presenti nell'invecchiamento e in vari disturbi cutanei. Viene citata per incrementare l'espressione delle sirtuine, proteine coinvolte nei meccanismi dell'invecchiamento. Sono state rilevate potenziali attività senolitiche e senomorfiche, oltre a benefici su parametri correlati all'obesità (glicemia a digiuno, insulino-resistenza, marcatori infiammatori). Le attività svolte dalla NAC permetterebbero di agire anche sulla disfunzione endoteliale e sui meccanismi patogenetici dell'aterosclerosi, nonché nelle malattie neurodegenerative.
La somministrazione intramuscolare ed endovenosa di GSH ha specifiche indicazioni cliniche. Al momento, solo in alcuni paesi asiatici, dove è diffusa la somministrazione endovenosa ad alti dosaggi per lo sbiancamento della pelle, le autorità sanitarie hanno richiamato l'attenzione sui possibili effetti collaterali e sull'assenza di studi su questo tipo d'impiego off-label.
8 modi per aumentare i livelli di Glutatione 📶
Le più recenti ricerche sottolineano l'importanza di conservare adeguati livelli di GSH cellulare per contrastare i meccanismi dell'invecchiamento e l'insorgenza di malattie correlate all'età. L'uso dei precursori del GSH, come la N-acetilcisteina (NAC) per via orale, si dimostra una scelta efficace e sicura, con nuove acquisizioni sulle attività geroprotettive. La NAC, in sinergia con altre molecole, contribuisce a mantenere e ristabilire l'omeostasi dei mitocondri e delle cellule sottoposte a molteplici sollecitazioni esogene ed endogene.
tags: #distemi #di #disintossicazione #glutatione #superossido