La sarcopenia, definita come una riduzione della massa muscolare e un compromesso della funzione muscolare, è associata a esiti avversi nella cirrosi. Gli amminoacidi a catena ramificata (BCAA) - che comprendono tre amminoacidi essenziali: leucina, isoleucina e valina - influenzano diversi pathways che portano alla perdita muscolare in questa popolazione. Uno studio randomizzato controllato in doppio cieco, pubblicato su Alimentary Pharmacology & Therapeutics, ha verificato se una supplementazione di BCAA potesse avere un impatto positivo sulle misure di sarcopenia nei pazienti con cirrosi.
La sarcopenia ha un’importante valenza prognostica nella cirrosi ed è un predittore indipendente di ridotta sopravvivenza, principalmente a causa della mortalità legata alla sepsi. La patogenesi della sarcopenia è multifattoriale e molti dei meccanismi che contribuiscono alla disfunzione e alla perdita muscolare sono specifici delle alterazioni emodinamiche, metaboliche e ormonali che accompagnano la cirrosi.
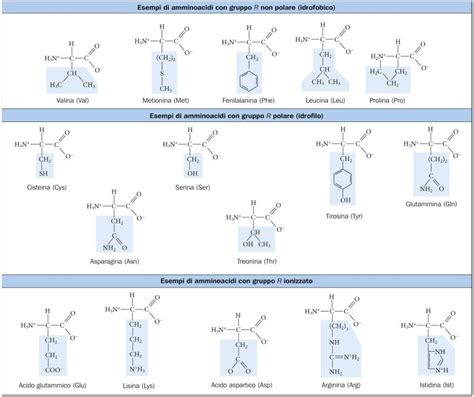
Gli amminoacidi a catena ramificata sono fondamentali per la produzione di energia, proteine e amminoacidi non essenziali. Inoltre, svolgono un ruolo cruciale nelle funzioni di segnalazione che promuovono la sintesi proteica e la crescita delle cellule muscolari. Nelle persone con cirrosi epatica, si osserva uno squilibrio tra gli amminoacidi, caratterizzato da bassi livelli circolanti di BCAA e livelli elevati di amminoacidi aromatici. Questo squilibrio è causato da una ridotta assunzione di proteine e da un aumento del catabolismo dei BCAA, attraverso la detossificazione dell’ammoniaca nei muscoli scheletrici e il loro uso come fonte di energia. Bassi livelli circolanti di BCAA sono associati a encefalopatia epatica, ipoalbuminemia e sarcopenia.
Studi sulla Supplementazione di BCAA nella Cirrosi
Gli autori hanno condotto uno studio randomizzato controllato in doppio cieco della durata di 12 mesi sulla supplementazione di BCAA rispetto a una proteina del siero di latte equicalorica ed equinitrogena in volontari con cirrosi epatica e ridotta forza muscolare. I volontari hanno ricevuto confezioni da 1 kg di BCAA in polvere o isolato di proteina del siero di latte. Il supplemento di BCAA conteneva 448 kJ e 26.3 g di proteine, inclusi 10.6 g di leucina, 5.3 g di isoleucina e 5.3 g di valina, per un contenuto totale di BCAA di 21.2 g. L’isolato di proteina del siero di latte conteneva 481 kJ e 26.6 g/giorno di proteine, con un contenuto totale di BCAA pari a 6 g.
La prescrizione di una dose giornaliera di 21.2 g di BCAA si è basata su linee guida internazionali per il dosaggio dei BCAA nelle malattie epatiche, pari a 0.25 g/kg/giorno. Nei volontari con un peso corporeo inferiore a 50 kg, è stato richiesto l’intervento di un dietista specializzato e la dose è stata ridotta in base al peso.
Endpoint dello Studio
L’endpoint composito primario era un aumento del 5% della forza di presa del lato non dominante (HGS) e/o della massa magra degli arti superiori (ULLM) misurata tramite assorbimetria a raggi X a doppia energia (DEXA). Questa valutazione è stata effettuata a 0, 6 e 12 mesi post-randomizzazione. Gli endpoint secondari includevano i cambiamenti nell’area del muscolo scheletrico (SMA) e nei parametri del tessuto adiposo, misurati tramite TC a singola sezione a livello della terza vertebra lombare (L3) a 0 e 12 mesi. L’effetto del trattamento sugli endpoint primari e secondari è stato valutato secondo il principio dell’intention-to-treat (ITT) ed è stato quantificato come la differenza media aggiustata tra i gruppi (MAD), con intervalli di confidenza al 95%, dal basale a 6 e 12 mesi rispettivamente, utilizzando un modello lineare misto per misure ripetute.
Risultati dello Studio
Lo studio ha reclutato 150 volontari: 74 partecipanti sono stati randomizzati per ricevere BCAA e 76 per ricevere il supplemento proteico di controllo. L’alcol era la causa più comune di cirrosi ed era responsabile della malattia epatica nel 40% dei volontari e un co-fattore per la malattia epatica in un ulteriore 13%. Non sono state notate differenze significative nell’eziologia della cirrosi tra i due gruppi.
Tra i volontari dello studio, 43 (28,7%) presentavano una malattia epatica classificata come Child-Pugh A, 51 (34%) avevano una malattia epatica classificata come Child-Pugh B, e 56 (37,0%) erano classificati come Child-Pugh C. Il punteggio mediano MELD (Model for End-Stage Liver Disease) era 14 [IQR 12; 17], senza differenze significative tra i due gruppi di studio.
Al basale, le misure della forza di presa e della massa magra degli arti superiori erano simili tra i gruppi di trattamento. A 6 mesi, 29 volontari (58,0%) nel gruppo BCAA e 27 volontari (51,9%) nel gruppo di controllo avevano raggiunto l’endpoint co-primario di un aumento del 5% della forza di presa e/o della massa magra degli arti superiori (p = 0,56). A 12 mesi, invece, l’endpoint primario è stato raggiunto dal 57% dei volontari nel gruppo BCAA e dal 61% nel gruppo di controllo (p = 0,80). Le persone che hanno raggiunto l’endpoint primario a 12 mesi avevano una malattia epatica più lieve rispetto a quelle che non lo hanno fatto. Gli autori hanno comunque sottolineato che la gravità della patologia era ben bilanciata tra i gruppi di trattamento. Esaminando indipendentemente ciascun endpoint, le variazioni di HGS e ULLM osservate tra i gruppi erano minime e statisticamente non significative (MAD a 12 mesi di 1,7 kg [IQR −0,2; 3,6] per la forza di presa e −0,15 kg [IQR −0,37; 0,06] per la massa magra degli arti superiori).
Per quanto riguarda gli endpoint secondari, a 6 e 12 mesi dall’arruolamento, non sono state osservate differenze significative nella massa magra appendicolare, o nella massa magra, tra i gruppi BCAA e di controllo. Lo studio non ha evidenziato differenze significative tra i gruppi a 12 mesi neanche nei parametri di composizione corporea misurati tramite TC a livello della terza vertebra lombare (L3), inclusi l’area del muscolo scheletrico (SMA), l’area del grasso sottocutaneo e l’area del grasso viscerale. Lo stesso discorso vale per la fragilità (indice di fragilità epatica e indice di fragilità di Fried), la batteria di test sulla performance fisica breve, i parametri biochimici ed ematologici, gli outcome clinici e la qualità di vita. La fatica è migliorata in tutta la coorte, senza differenze significative tra i gruppi. Il 15% dei volontari ha riportato effetti collaterali, con un maggiore disgusto nel gruppo BCAA (p = 0.045).
È stata effettuata inoltre un’analisi per protocollo basata sui partecipanti che hanno completato lo studio e che sono stati ritenuti compliant durante tutto il periodo di follow-up. Questa analisi è stata ulteriormente stratificata per sesso. Anche in questo caso, non sono state rilevate differenze significative tra i gruppi in termini di sarcopenia, fragilità o parametri di performance, così come per altri parametri.
Limiti ed Evidenze Emergenti
Secondo i ricercatori, il principale limite di questo studio è costituito dall’elevato tasso di abbandono, superiore alle aspettative, anche se i partecipanti che non lo hanno completato erano distribuiti in modo equilibrato tra i gruppi di trattamento. Gli autori ritengono che ciò rifletta la difficoltà intrinseca nello studiare persone con malattia epatica allo stadio terminale, che spesso progrediscono verso il decesso o necessitano di un trapianto di fegato.
Nonostante i limiti, questo trial randomizzato controllato in doppio cieco ha evidenziato che la supplementazione di BCAA non ha sostanzialmente migliorato le misure di sarcopenia, fragilità o qualità della vita in volontari con cirrosi e debolezza muscolare rispetto a una supplementazione proteica standard a base di siero di latte.

Tuttavia, altre evidenze suggeriscono che l'integrazione con BCAA in caso di malattia epatica cronica (ACLD) avanzata può considerarsi un trattamento sicuro, con effetti positivi sul decorso clinico dell'encefalopatia epatica (HE) e della sarcopenia, tra le complicanze più gravi dell'ACLD, e può anche migliorare la sopravvivenza. L'ACLD rappresenta uno stadio avanzato della malattia epatica, caratterizzato da fibrosi, noduli rigenerativi e cirrosi, con compromissione della funzionalità del fegato. Quadri di malnutrizione si associano a sviluppo di complicanze, ridotta sopravvivenza e ridotta qualità della vita.
“Nei pazienti affetti da sarcopenia, l’integrazione con BCAA ha un effetto positivo su massa e forza muscolare e sui livelli di albumina, che può portare a un miglioramento della sopravvivenza” si sottolinea nelle conclusioni del lavoro. “Gli effetti benefici dei BCAA sono amplificati quando vengono utilizzati in combinazione con l'esercizio fisico e l'intervento nutrizionale. Questa evidenza potrebbe supportare potenzialmente l’uso di integratori di BCAA nella pratica clinica, in combinazione con trattamenti standard, soprattutto nei sottogruppi di pazienti con concomitante HE e sarcopenia. È necessario identificare i pazienti che potrebbero trarre un maggiore beneficio dall’intervento nutrizionale precoce e dall’integrazione. La somministrazione orale sembra essere più efficace di quella endovenosa e andrebbe preferita. Una dose minima di 12 g/die per via orale è più efficace rispetto a dosi inferiori, ma sono necessari ulteriori studi per valutare dose e durata più adeguate del trattamento. È plausibile ipotizzare che gli effetti benefici osservati possano essere mediati da un miglioramento dello stato nutrizionale, potenzialmente dovuto, a sua volta, a un miglioramento della funzionalità epatica. Nel complesso, l’uso dei BCAA nella malattia epatica cronica avanzata è un trattamento sicuro che può avere effetti positivi sul decorso clinico dell’HE e della sarcopenia e può anche migliorare la sopravvivenza.”
La supplementazione dietetica con aminoacidi a catena ramificata (BCAA) dopo un episodio di encefalopatia epatica (HE) non riduce la recidiva di HE ma migliora la HE minima e la massa muscolare. In ogni caso, l'identificazione dei fattori di rischio per la recidiva di HE può consentire lo sviluppo di nuove terapie preventive che potrebbero ridurre le sequele neuropsicologiche causate da ripetuti episodi di HE. Queste le conclusioni di una multicentrica randomizzata in doppio cieco condotta da Iñigo Les, dell'hospital Vall d'Hebron di Barcellona, e da altri autori spagnoli, su 116 pazienti con cirrosi e un precedente episodio di HE. Tutti i pazienti hanno ricevuto la dieta standard (35 kcal/kg al giorno e 0,7 g di proteine per kg al giorno) insieme a un supplemento di 30 g di BCAA oppure maltodestrina (Mdx) nel corso di 56 settimane. Il rischio attuariale di non incorrere in HE non differiva tra i due gruppi (BCAA = 47%, Mdx = 34%, ma i pazienti nel primo gruppo hanno mostrato un risultato migliore dopo l'esecuzione di due test neuropsicologici e un incremento della circonferenza muscolare a livello del braccio. La recidiva è apparsa associata a bassi livelli di albumina plasmatica al basale, e a una riduzione del sodio e un incremento della creatinina nel corso del follow-up.
Aminoacidi Ramificati BCAA: cosa sono? a che cosa servono?
Gli aminoacidi ramificati sono proposti per contrastare l’affaticamento, migliorare la concentrazione e le performance atletiche e ridurre la perdita di massa muscolare durante l'esercizio. Inoltre sono utilizzati in caso di SLA, problemi cerebrali associati a malattie epatiche, discinesia tardiva, perdita dell'appetito in anziani con insufficienza renale o pazienti oncologici, malattia di McArdle e degenerazione spinocerebellare.
I disturbi del metabolismo degli aminoacidi a catena ramificata (BCAA) costituiscono un gruppo di malattie metaboliche ereditarie caratterizzate dall'incapacità dell'organismo di scomporre correttamente tre aminoacidi essenziali: la leucina, l'isoleucina e la valina. Queste condizioni, se non diagnosticate e trattate precocemente, possono portare a gravi danni neurologici, disabilità permanenti o esiti fatali. Il trattamento deve essere iniziato immediatamente dopo la diagnosi e prosegue per tutta la vita.
L’insufficienza epatica può essere lieve, moderata o grave, e presentarsi, durante un’epatite, sotto forma acuta o cronica. L’insufficienza epatica si caratterizza per una riduzione delle funzioni dell’organo. Nelle forme lievi, può essere mantenuta l’alimentazione tradizionale e non occorre la nutrizione artificiale. Sono consigliati pasti leggeri, con porzioni moderate, senza trascurare l’apporto nutrizionale complessivo. Nell’insufficienza epatica moderata e ancor più nella grave, laddove necessitano talvolta nutrizione enterale o parenterale, si richiedono accorgimenti quali l’esclusione del sale dalla dieta, per ridurre la tendenza all’edema e all’ascite, e la moderazione della quota proteica, con un supplemento di amminoacidi ramificati, i quali non richiedono metabolizzazione epatica prima dell’ossidazione cellulare, e hanno un bassissimo livello di scorie azotate (a loro volta responsabili dell’insorgenza di encefalopatia epatica).
| Parametro | Gruppo BCAA (n=74) | Gruppo Controllo (Proteine Siero Latte) (n=76) | Valore p |
|---|---|---|---|
| Endpoint Primario (a 6 mesi): Aumento 5% HGS e/o ULLM | |||
| Volontari che hanno raggiunto l'endpoint | 58.0% | 51.9% | 0.56 |
| Endpoint Primario (a 12 mesi): Aumento 5% HGS e/o ULLM | |||
| Volontari che hanno raggiunto l'endpoint | 57% | 61% | 0.80 |
| Variazione Media Aggiustata (MAD) a 12 mesi (vs basale) | |||
| Forza di Presa (kg) | 1.7 [IQR -0.2; 3.6] | - | - |
| Massa Magra Arti Superiori (kg) | -0.15 [IQR -0.37; 0.06] | - | - |
| Effetti Collaterali | |||
| Percentuale volontari con effetti collaterali | 15% (con maggiore disgusto) | - | 0.045 (per disgusto) |
Le informazioni contenute in questo articolo sono a scopo puramente divulgativo e non sostituiscono in alcun modo il parere medico professionale. Prima di integrare nella dieta gli aminoacidi ramificati, è consigliabile un consulto medico.
tags: #aminoacidi #ramificati #sconsigliate #nel #encefalopatia