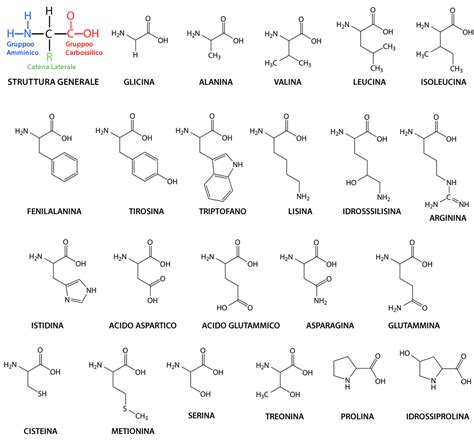
Gli amminoacidi (o aminoacidi, AA) rappresentano le unità strutturali fondamentali che costituiscono le proteine. La loro diversità deriva dalle catene laterali, indicate con il gruppo R, che conferiscono a ciascun amminoacido proprietà uniche.
Classificazione degli Amminoacidi
La configurazione assoluta degli zuccheri e degli amminoacidi semplici viene determinata utilizzando il sistema D-L, che si basa sulla configurazione assoluta della gliceraldeide. Negli organismi viventi, le molecole chirali sono tipicamente presenti in una sola delle due forme; nel caso degli amminoacidi, in natura si trovano prevalentemente gli isomeri L.
Gli amminoacidi possono essere suddivisi in diverse categorie in base alla natura del loro gruppo R:
- Amminoacidi con gruppo R non polare alifatico: Questo gruppo include amminoacidi caratterizzati da catene laterali apolari. La glicina, con la sua catena laterale costituita da un singolo atomo di idrogeno, è l'amminoacido più semplice. La prolina si distingue per la sua peculiare struttura ad anello.
- Amminoacidi con gruppo R aromatico: Le catene laterali aromatiche possono partecipare a interazioni idrofobiche, influenzando la struttura tridimensionale delle proteine.
- Amminoacidi con gruppo R polare ma non carico: Questi amminoacidi presentano catene laterali polari che possono formare legami idrogeno.
- Amminoacidi con gruppo R carico positivamente (basici): Questi amminoacidi possiedono gruppi R che, a pH fisiologico, sono carichi positivamente.
- Amminoacidi con gruppo R carico negativamente (acidi): Questi amminoacidi presentano gruppi R che, a pH fisiologico, sono carichi negativamente.
Proprietà Chimico-Fisiche degli Amminoacidi
Ciascun amminoacido possiede un valore di punto isoelettrico (pI), che corrisponde al valore di pH al quale l'amminoacido esiste prevalentemente in forma zwitterionica, ovvero con carica netta pari a zero. Il pK rappresenta il valore di pH in cui la forma dissociata e la forma indissociata di un gruppo funzionale sono presenti in concentrazioni equimolecolari. Il pH, d'altra parte, indica la concentrazione di ioni H+ in una soluzione.
Una caratteristica fondamentale degli amminoacidi è la loro capacità di agire sia come acidi che come basi. Quando un amminoacido è sciolto in acqua, forma uno ione dipolare, noto come zwitterione. Uno zwitterione può comportarsi da acido, donando protoni, o da base, accettando protoni.
La carica netta di un peptide è determinata dalla somma algebrica delle cariche presenti sui gruppi carbossilico e amminico terminali, nonché di ogni gruppo ionizzabile presente nelle catene laterali degli amminoacidi che lo compongono.
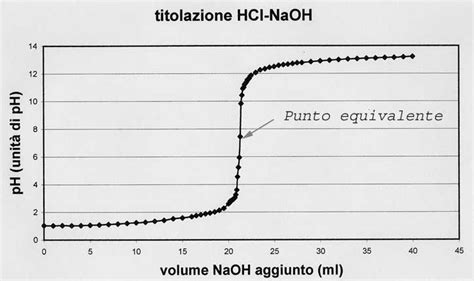
In una soluzione acida, ad esempio a pH=1, il gruppo carbossilico (COOH) rimane non ionizzato, mentre il gruppo amminico si presenta protonato (NH3+). All'aumentare del pH, il gruppo carbossilico è il primo a cedere un protone, trasformandosi in COO-.
Gli amminoacidi che possiedono un singolo gruppo amminico α, un singolo gruppo carbossilico α e un gruppo R non ionizzabile mostrano curve di titolazione simili a quelle della glicina. Al contrario, gli amminoacidi con un gruppo R ionizzabile presentano curve di titolazione più complesse, con tre fasi distinte che corrispondono alle tre possibili tappe di ionizzazione, e di conseguenza, tre valori di pK.
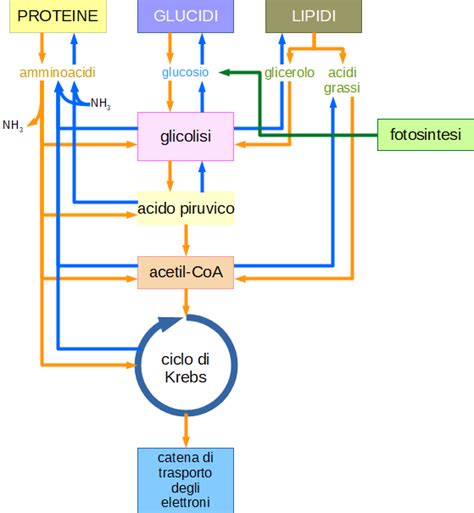
Il metabolismo degli amminoacidi
Rilevanza per la Biochimica e il Benessere Animale
La comprensione della struttura e della funzione delle biomolecole, incluse le principali vie metaboliche degli zuccheri, dei lipidi e degli amminoacidi, è essenziale per la formazione di un esperto di benessere animale. Lo studente dovrà acquisire una solida conoscenza dei concetti di base della biochimica, con particolare attenzione alla termodinamica chimica e alla cinetica enzimatica.
È fondamentale che lo studente sia in grado di collegare e integrare le conoscenze acquisite con quelle di corsi precedenti e successivi, sviluppando capacità di apprendimento continuo e di aggiornamento nell'ambito della biochimica. La familiarità con la struttura, l'attività catalitica e regolatoria degli enzimi, così come con le principali vie metaboliche delle maggiori specie animali, è di cruciale importanza.
tags: #suddivisione #aminoacidi #lemimgher