L'acido L-ascorbico, comunemente noto come vitamina C, è un composto chimico fondamentale con un ruolo cruciale in numerosi processi biologici. La sua importanza è stata riconosciuta fin dall'antichità, legata alla prevenzione dello scorbuto, una patologia da carenza. La storia della sua scoperta e comprensione è un percorso affascinante che attraversa secoli di ricerca scientifica.
Storia e Scoperta
La storia dell'acido ascorbico è intrinsecamente legata a quella dello scorbuto, una malattia legata a una carenza di questo composto nella dieta. Questa malattia era già descritta nella medicina greca attorno al V secolo a.C. Tuttavia, la prima prova scientifica venne nel maggio del 1747 da parte di James Lind, un chirurgo della marina reale inglese. Lind sottopose a un esperimento 12 membri dell'equipaggio affetti da scorbuto, dividendoli in sei gruppi da due persone ciascuno. A ogni gruppo fece assumere, oltre alle normali razioni alimentari, un composto particolare: sidro, acido solforico, aceto, spezie ed erbe, acqua di mare, arance e limoni. I risultati ottenuti permisero di dimostrare che effettivamente quest'ultima aggiunta permetteva di prevenire l'insorgere dello scorbuto. Lind pubblicò i risultati di questo studio nel 1753.
Nel XVIII e XIX secolo venne usato il termine di antiscorbutico per tutti quei cibi che erano in grado di prevenire la comparsa dello scorbuto. Tra essi, oltre ai limoni, alle arance e ai lime, vi sono: i crauti, il cavolo salato, il malto e il brodo portatile. Nel 1912 Casimir Funk, da studi su malattie carenziali, ipotizzò la presenza di composti che denominò vitamine. Nel 1921 il composto antiscorbutico venne denominato vitamina C e tra il 1928 e 1933 fu isolato e cristallizzato da Joseph Svirbely e dall'ungherese Albert Szent-Gyorgyi Von Nagyrapolt e, in modo indipendente, da Charles Glen King. Nel 1934 Sir Walter Norman Haworth e Tadeusz Reichstein, in maniera indipendente, riuscirono a sintetizzare la vitamina C. Nel 1937 Szent-Gyorgyi ricevette il Premio Nobel per la medicina per le sue scoperte sui processi biologici di combustione, con particolare riguardo alla vitamina C, e alla catalisi dell'acido fumarico.
Struttura Chimica e Proprietà
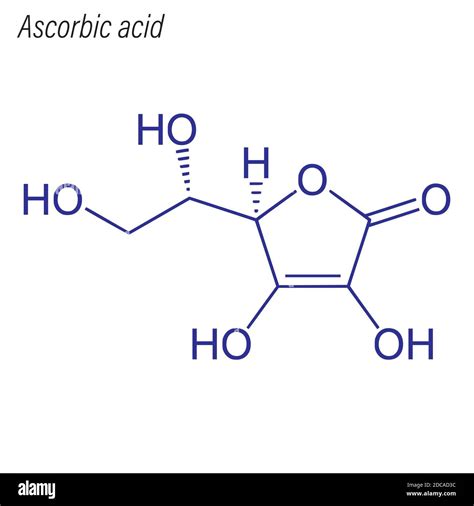
L'acido ascorbico (acido L-ascorbico) è un composto chimico, una vitamina C sintetizzata. Mentre la vitamina C è un composto organico, l'acido ascorbico è la forma più pura di vitamina C, ma è un composto chimico, una forma sintetizzata di vitamina C. Entrambi hanno la stessa formula molecolare C6H8O6 o Hc6H7O6. Il peso molecolare è di 176.12 g/mol. Il suo numero CAS è 50-81-7.
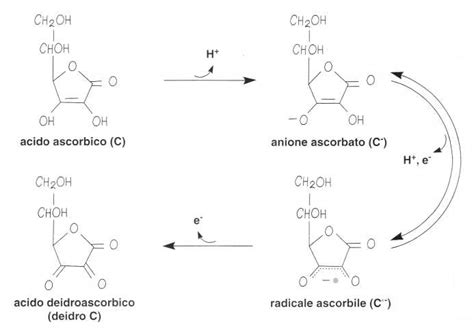
In condizioni fisiologiche e a pH 7, la vitamina C si trova in forma dissociata, cioè come monoelettrone riducente. Questo avviene perché il gruppo -OH enolico legato al C2 dell'anello lattonico possiede una pKa di 4,2, che lo rende debolmente acido. A pH 7, vicino al pH del plasma, la forma predominante della vitamina C è il monoanione ascorbato, seguita dall'acido ascorbico e, in concentrazioni molto basse, dal dianione ascorbato (0,005%).
L'acido ascorbico è facilmente ossidato da ossigeno, alcali e alte temperature. Reagisce come un agente riducente relativamente forte e decolora molti coloranti. Forma sali metallici stabili. È incompatibile con ossidanti, coloranti, alcali, ferro e rame.
Sintesi dell'Acido Ascorbico
Il percorso dell'acido uronico consente alla maggior parte delle piante e degli animali di sintetizzare l'ascorbato a partire da glucosio o galattosio attraverso l'azione della gluconolattone ossidasi. Il corpo umano ha sviluppato un efficace sistema di adattamento che mantiene le riserve organiche di vitamina C e ne previene la carenza a causa di un basso apporto dietetico. Questi adattamenti includono una maggiore capacità di assorbimento e riciclo della vitamina C rispetto ad altre specie animali.
La sintesi dell'acido ascobico può avvenire attraverso diversi processi. La sintesi classica di Reichstein - Grüssner inizia con la riduzione del D-glucosio a D-sorbitolo mediante idrogenazione su un catalizzatore di nichel. Segue l'ossidazione microbiologica del D-sorbitolo a L-sorbosio effettuata con *A. xylinum*. La protezione del di-O-isopropilidenile dei gruppi ossidrilici in C-2, C-3 e C-4, C-6 consente un'ossidazione ad alta resa in acido di-O-isopropilidene-2-cheto-gulonico, evitando sovra-ossidazioni o altre reazioni indesiderate. Segue il trattamento dell'acido di-O-isopropilidene-2-cheto-gulonico con acqua calda che produce acido 2-cheto-L-gulonico, il quale viene convertito in acido L-ascorbico mediante riscaldamento in acqua a 100 °C (resa del 20%) oppure per esterificazione e successivo trattamento con metossido di sodio in metanolo seguito da acidificazione con acido cloridrico, ottenendo circa il 70% di acido L-ascorbico.
Un altro processo industriale prevede diverse fasi: fermentazione del glucosio a sorbitolo, ossidazione a sorbosio, isomerizzazione ad acido chetogulonico, ossidazione e idrolisi ad acido 2-cheto-L-gulonico, riduzione ad acido ascorbico e infine purificazione attraverso cristallizzazione, filtrazione ed essiccazione.
Determinazione e Analisi
Esistono diversi metodi per determinare la quantità di vitamina C in varie sostanze. Uno di questi sfrutta il potere riducente della vitamina C e utilizza il 2,6-diclorofenolindofenolo (DCIP) come indicatore redox per la determinazione dell'acido ascorbico. Il principio di questo metodo consiste in una titolazione dell'acido ascorbico con diclorofenolindofenolo. L'acido ascorbico reagisce con il DCPIP, cambiando colore da blu a incolore. I campioni alimentari vengono estratti utilizzando acido metafosforico (MPA) e il pH viene regolato a 1,2. Il punto finale di questa titolazione si raggiunge quando la soluzione assume una colorazione rosa dovuto all'eccesso di colorante non ridotto in soluzione acida.
È possibile determinare la quantità di vitamina C anche attraverso l'utilizzo del reattivo di Lugol. Lo iodio ossida con facilità l'acido ascorbico convertendolo in acido deidroascorbico. Nelle analisi quantitative il campione di acido ascorbico viene trattato con una quantità nota di iodio superiore a quella necessaria a ossidare l'intero campione; l'eccesso di iodio non reagito viene quindi retrotitolato con una soluzione a concentrazione nota di tiosolfato di sodio.
La spettrofotometria UV è un altro metodo frequentemente utilizzato per determinare la concentrazione dell'acido ascorbico, poiché il composto è in grado di assorbire i raggi UV ed è un metodo semplice. Un altro metodo è quello enzimatico: l'ascorbato ossidasi catalizza l'ossidazione dell'acido ascorbico in acido deidroascorbico. Il DHAA formato reagisce con o-fenilendiammina per produrre 2,2-anidrochinoxalina di cui si osserva l'assorbimento rispetto a un bianco appositamente preparato a 358 nm.
La preparazione e l'estrazione del campione sono passaggi importanti per minimizzare la degradazione dell'acido ascorbico (AA). L'MPA è il reagente più comunemente utilizzato, poiché può funzionare sia come agente estrattivo che stabilizzante. Inibisce l'ascorbato ossidasi, la catalisi dei metalli e precipita le proteine. L'MPA può essere usato con altri acidi organici e modificatori come acido acetico, metanolo, ecc., oltre a stabilizzanti come l'EDTA e il glutammato monosodico (MSG). L'AA ha una stabilità maggiore nell'MPA rispetto all'acido ossalico e all'acido tricloroacetico.
Ruolo Biologico e Funzioni
L'acido ascorbico è essenziale per la sintesi e il metabolismo della vitamina B9 e della tirosina. La prolina e la glicina vengono anch'esse idrossilate con il suo aiuto. Facilita il metabolismo delle catecolamine, della carnitina e della lisina. Inoltre, l'acido ascorbico favorisce la conversione del colesterolo in acidi biliari, riducendo i livelli di colesterolo nel sangue. Sembra inoltre che la vitamina C possa diminuire la formazione di nitrosammine intestinali e ridurre vari composti ossidanti tra cui il radicale superossido, l'acido ipocloroso e i radicali idrossilici.
La capacità dell'ascorbato di donare elettroni gli permette di agire come un agente di eliminazione dei radicali liberi e di ridurre stati di ossidazione più elevati del ferro a Fe²⁺. Nel corpo umano è utilizzata per il mantenimento delle difese antiossidanti della cellula, è uno spazzino di radicali liberi. Svolge anche l'importante funzione di contribuire alla rigenerazione della vitamina E. La vitamina C passa anche da una forma ossidata (acido L-deidroascorbico) a una forma ridotta (acido L-ascorbico). Inoltre, la vitamina C è importante per l'assorbimento e il metabolismo del ferro.
L'acido ascorbico non è solo un antiossidante, ma ha alcune peculiarità biosintetiche in diversi organismi come co-substrato di diverse diossigenasi, una funzione particolare nell'espressione genica, il ruolo importante degli enzimi rigenerativi, modulatore del metabolismo neuronale. Gioca un ruolo chiave nella difesa antiossidante endogena ed è cofattore nella produzione di carnitina e collagene.
L'incredibile potere ANTICANCRO della VITAMINA C...oppure no? Ne parla un oncologo
Carenza e Patologie
La carenza di vitamina C determina la comparsa dello scorbuto, patologia che riguarda particolarmente l'insufficiente produzione di collagene e di sostanza cementante intercellulare. Ciò determina alterazioni a livello dei vasi sanguigni con comparsa di emorragie, rallentamento della cicatrizzazione delle ferite, gengiviti con alterazioni della dentina, gengivorragie e osteoporosi. Nei bambini si ha anche un arresto della crescita.
Bassi livelli di acido ascorbico sufficienti alla sopravvivenza, ma al di sotto di quelli necessari, sembrano favorire l'aterosclerosi, sia per l'ipotesi ossidativa sia per l'ipotesi risposta alla lesione. L'insufficienza di acido ascorbico può verificarsi in condizioni di stress ossidativo sistemico, infiammazione, sepsi, trauma.
Applicazioni e Usi
L'acido ascorbico viene usato per trattare la carenza di vitamina C, lo scorbuto, la guarigione ritardata delle ferite e delle ossa, l'acidificazione delle urine, nella prevenzione e nel trattamento dell'anemia sideropenica e in generale come antiossidante.
In medicina, l'acido ascorbico è studiato per il trattamento e la prevenzione del cancro, con inibizione della crescita delle cellule di cancro alla prostata, alle ovaie e al pancreas, delle cellule di neuroblastoma e inibizione della crescita e delle metastasi del cancro al fegato. Viene anche usato nel trattamento del raffreddore e dell'influenza.
Nell'alimentazione, viene aggiunto alla farina per migliorarne l'assorbimento dell'acqua con conseguente aumento del volume e un migliore controllo del prodotto durante la lievitazione. Ha il numero E300 nella lista degli additivi alimentari europei come antiossidante.
In cosmetica, agisce come agente antiossidante, contrastando lo stress ossidativo e prevenendo danni cellulari. Funge anche da agente tampone, stabilizzando il pH delle soluzioni, e può contribuire alla fragranza e agire come agente condizionante della pelle, prevenendo la disidratazione.
Il corpo non è in grado di produrre da solo la vitamina C e non la immagazzina, pertanto è importante ottenerla quotidianamente da fonti alimentari come agrumi, kiwi, fragole, e verdure.

Stabilità e Degradazione
L'acido ascorbico è sensibile all'esposizione prolungata alla luce e all'aria. È sensibile all'umidità ed è soggetto a degradazione in condizioni anaerobiche. La degradazione della vitamina C può avvenire attraverso percorsi anaerobici e aerobici.
I prodotti commerciali contenenti acido ascorbico devono soddisfare condizioni di qualità, sicurezza ed efficacia per tutta la loro vita utile. La stabilità è fondamentale e può essere compromessa da reazioni chimiche dovute al basso rapporto principio attivo/eccipiente, ai cambiamenti delle particelle e all'effetto dell'ambiente (temperatura, umidità, luce e ossigeno). I test di stabilità aiutano a determinare la stabilità intrinseca della molecola e a identificare i prodotti di degradazione.
La stabilità e la solubilità del prodotto devono essere verificate in diversi tipi di acqua e a diverse temperature, simulando situazioni reali. È necessario specificare la solubilità massima del prodotto e misurare la torbidità. Va inoltre verificato che la presenza di cloro nell'acqua non comporti fenomeni che agiscano negativamente sulla stabilità della molecola.
La conservazione prolungata può influire sulla qualità del farmaco (appetibilità e contaminazione). I fattori associati a prodotti che non sono stabili in acqua si traducono in scarsa biodisponibilità, incapacità di ottimizzare i componenti attivi, mancanza di risposta proporzionale alla dose, dosaggi non ottimali e precipitazione incontrollabile dopo la somministrazione.
Considerazioni sugli Integratori
Nel campo dell'integrazione alimentare, gli integratori a base di vitamina C sono molto popolari. La vitamina C è un nutriente essenziale per il corretto funzionamento di numerose funzioni biologiche, tra cui la sintesi del collagene, la guarigione delle ferite e il supporto al sistema immunitario.
Esiste una differenza tra acido ascorbico e ascorbato di sodio. L'acido ascorbico, in quanto acido, può risultare sgradevole al gusto e mal tollerato a livello gastrico. L'ascorbato di sodio, un sale dell'acido L-ascorbico, possiede un sapore più gradevole e neutro, ed è raccomandato per chi soffre di problemi gastrici con l'acido ascorbico. Tuttavia, l'ascorbato di sodio è controindicato in soggetti che seguono diete povere di sodio.
La soluzione con il miglior rapporto costi/benefici è spesso rappresentata dall'acido ascorbico puro. Ad esempio, un integratore di Acido Ascorbico puro in polvere fornisce 1 g di vitamina C per 1 g di prodotto.
Sia l'ascorbato di sodio che l'acido ascorbico sono molecole osmoticamente attive. La somministrazione di vitamina C per via orale come forma farmaceutica solida (compresse) è stata associata a danni esofagei dovuti all'acidificazione.
La vitamina C può provocare emolisi nei pazienti con carenza eritrocitaria di G6PD o favismo. L'assunzione per via orale è considerata sicura quando rispetta i dosaggi raccomandati, ma potrebbe essere controindicata in caso di angioplastica, tumori, diabete, malattie ematologiche, calcoli renali, infarto, carenza di G6PD, anemia mediterranea e in fumatori.
Tabella 1. Caratteristiche tipiche del prodotto commerciale di Acido Ascorbico
| Caratteristica | Valore |
|---|---|
| Aspetto | Polvere cristallina bianca o quasi bianca o cristalli incolori |
| Purezza (saggio) | ≥99% |
| Punto di fusione | Circa 190℃ (con decomposizione) |
| pH (soluzione acquosa al 5%) | 2.1-2.6 |
| pH (soluzione acquosa al 2%) | 2.4-2.8 |
| Rotazione ottica specifica | 20.5℃- 21.5℃ |
| Perdita all'essiccamento | ≤0.4% |
| Impurezza E | ≤0.2% |
| Impurezze totali | ≤0.20% |
| Rame | ≤5.0ppm |
| Ferro | ≤2.0ppm |
| Arsenico | ≤3.0ppm |
| Piombo | ≤2.0ppm |
| Mercurio | ≤1.0ppm |
| Cadmio | ≤1.0ppm |
| Metalli pesanti | ≤10ppm |
| Residuo solfatato | ≤0.1% |
Formula molecolare: C6H8O6
Peso molecolare: 176.12 g/mol
Sinonimi: L(+)-Ascorbic acid, l-ascorbic acid, vitamin C