La "leucine zipper" (o forbici di leucina) è un comune motivo strutturale tridimensionale nelle proteine. Questo motivo è stato descritto per la prima volta da Landschulz e collaboratori nel 1988, quando scoprirono che una proteina legante enhancer possedeva un segmento caratteristico di 30 amminoacidi. L'esposizione di queste sequenze amminoacidiche su un'ideale alfa-elica rivelò una ripetizione periodica di residui di leucina in ogni settima posizione, coprendo una distanza di otto giri elicoidali.
Le leucine zipper sono un motivo di dimerizzazione della classe bZIP (Basic-region leucine zipper) dei fattori di trascrizione eucariotici. Il dominio bZIP ha una lunghezza di 60-80 amminoacidi, con una regione basica altamente conservata per il legame al DNA e una regione di dimerizzazione della leucine zipper più diversificata. La localizzazione delle leucina è fondamentale per il legame del DNA alle proteine.
Le leucine zipper sono presenti sia nelle proteine regolatrici eucariotiche che procariotiche, ma sono principalmente una caratteristica degli eucarioti. Un altro dominio di legame al DNA, il dimero Helix-loop-helix (HLH), è mostrato legato a un frammento di DNA, dove ogni alfa-elica rappresenta un monomero. La leucine zipper viene creata dalla dimerizzazione di due specifiche alfa-eliche monomeriche legate al DNA.
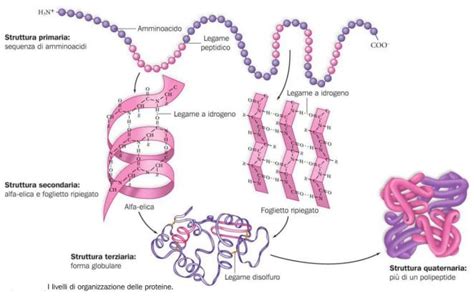
La leucine zipper è formata dall'interazione anfipatica tra due domini ZIP. Il dominio ZIP si trova nell'alfa-elica di ciascun monomero e contiene leucina o amminoacidi simili alla leucina. Questi amminoacidi sono distribuiti nella sequenza polipeptidica di ciascuna regione in modo tale che, quando la sequenza si avvolge in una alfa-elica 3D, i residui di leucina si allineano sullo stesso lato dell'elica. Questa regione dell'alfa-elica, contenente le leucina che si allineano, è chiamata dominio ZIP, e le leucina di ciascun dominio ZIP possono interagire debolmente con le leucina di altri domini ZIP, tenendo insieme le loro alfa-eliche in modo reversibile (dimerizzazione). Quando queste alfa-eliche si dimerizzano, si forma la zipper.
Il lato idrofobico dell'elica si accoppia con sé stesso o con un'altra elica simile, nascondendo gli amminoacidi non polari lontano dal solvente. I motivi di leucine zipper sono considerati un sottotipo di "coiled coil", che sono costruiti da due o più alfa-eliche avvolte l'una intorno all'altra per formare una superelica. Le "coiled coil" contengono ripetizioni di 3 e 4 residui la cui idrofobicità e composizione di residui sono compatibili con la struttura di alfa-eliche anfipatiche. Nel caso delle leucine zipper, le leucina sono predominanti nella posizione 'd' della ripetizione eptadica. Questi residui si impacchettano ogni due giri delle alfa-eliche, e la regione idrofobica tra le due eliche è completata da residui nelle posizioni 'a', che sono anch'essi frequentemente idrofobici. Vengono definite "coiled coil" a meno che non sia dimostrata la loro importanza per la funzione proteica.

Due diversi tipi di queste alfa-eliche possono accoppiarsi per formare una leucine zipper eterodimerica. Il bZIP interagisce con il DNA tramite residui basici e amminici (vedi amminoacidi basici nella tabella fornita, ordinati per pH) nel dominio "basico", come lisina e arginina. Questi residui basici interagiscono nel solco maggiore del DNA, formando interazioni specifiche di sequenza.
Il meccanismo di regolazione trascrizionale da parte delle proteine bZIP è stato studiato in dettaglio. La maggior parte delle proteine bZIP mostra un'elevata affinità di legame per i motivi ACGT, che includono CACGTG (G box), GACGTC (C box), TACGTA (A box), AACGTT (T box) e un motivo GCN4, ovvero TGA(G/C)TCA. Gli eterodimeri bZIP esistono in una varietà di eucarioti e sono più comuni negli organismi con maggiore complessità evolutiva. Gli eterodimeri bZIP differiscono dagli omoodimeri bZIP e tra loro per l'affinità di interazione proteina-proteina. Questi eterodimeri esibiscono una complessa specificità di legame al DNA. Quando combinati con un partner diverso, la maggior parte delle coppie bZIP si lega a sequenze di DNA che ciascun partner individuale preferisce. In alcuni casi, la dimerizzazione di diversi partner bZIP può alterare la sequenza di DNA che la coppia bersaglia in un modo che non poteva essere previsto basandosi sulle preferenze di ciascun partner da solo. Ciò suggerisce che, come eterodimeri, i fattori di trascrizione bZIP sono in grado di modificare le loro preferenze riguardo alla localizzazione che bersagliano nel DNA. Un piccolo numero di fattori bZIP, come OsOBF1, può anche riconoscere sequenze palindrome. Tuttavia, altri, tra cui LIP19, OsZIP-2a e OsZIP-2b, non si legano a sequenze di DNA.
Le proteine regolatrici con leucine zipper includono c-fos e c-jun (il fattore di trascrizione AP1), importanti regolatori dello sviluppo normale, così come i membri della famiglia myc, tra cui myc, max e mxd1.
La proteina nucleare NFIL3 (Nuclear factor interleukin 3 regulated protein), contenente bZIP, è un repressore trascrizionale che svolge molteplici ruoli nella regolazione di vari processi biologici. La proteina NFIL3 è composta da 462 amminoacidi, incluso un dominio bZIP. La porzione N-terminale del dominio contiene il motivo basico, che si lega direttamente al DNA. L'espressione del gene Nfil3 cambia insieme al ciclo circadiano e NFIL3, come fattore di repressione, regola il ritmo circadiano. NFIL3 compete con l'attivatore trascrizionale D site albumin promoter binding protein (DBP) nel legame con gli elementi D box nel DNA, che sono uno dei siti consenso dei fattori di trascrizione circadiani. DBP è un'altra proteina bZIP e mostra un profilo di espressione opposto a quello di NFIL3. Quando il livello di NFIL3 è alto, i geni sotto il controllo degli elementi D box vengono repressi.
NFIL3 influenza la sopravvivenza cellulare ed è coinvolto nell'oncogenesi. NFIL3 è un fattore di sopravvivenza che ostacola la morte cellulare apoptotica in numerosi tipi cellulari e porta all'oncogenesi. Un alto livello di espressione di NFIL3 è associato al cancro al seno. Nelle cellule tumorali, NFIL3 si associa alla Istone Deacetilasi 2 (HDAC2) e reprime geni pro-apoptotici come Tumor necrosis factor ligand superfamily member 10 (TRAIL) e TNF receptor superfamily member 6 (FAS) per prevenire l'apoptosi. NFIL3 può anche ostacolare l'apoptosi nelle cellule tumorali legandosi al DNA e bloccando l'accesso del fattore di trascrizione Forkhead box O1 (FOXO1) ai geni di morte cellulare, il che compromette il ciclo cellulare e promuove l'oncogenesi.
NFIL3 agisce come repressore per i geni associati alla rigenerazione neuronale. Nfil3 è espresso nelle cellule neuronali con potenziale rigenerativo per mantenere sotto controllo la crescita cellulare. L'espressione di Nfil3 è indotta dal cAMP-response element binding protein (CREB) fosforilato, e la proteina NFIL3 a sua volta compete per i siti di legame condivisi con CREB e CCAAT/Enhancer Binding Protein (CEBP), riducendo l'espressione dei geni bersaglio di CREB e CEBP per contrastare l'effetto del segnale cAMP. NFIL3 è anche importante in immunologia.
La regolazione dell'espressione genica
tags: #dimerizzaziobe #leucine #zipper