L'ossido di magnesio, noto anche come magnesia bruciata o semplicemente magnesia, è un composto chimico inorganico. Appartiene al gruppo degli ossidi basici. L'ossido di magnesio è presente in natura come minerale periclasio. Si ottiene bruciando il magnesio o arrostendo la magnesite (carbonato di magnesio) o la dolomite. L'ossido di magnesio può essere prodotto anche per calcinazione (riscaldamento di un composto chimico al di sotto del suo punto di fusione per provocare una parziale decomposizione chimica) del carbonato di magnesio o dell’idrossido di magnesio. L’idrossido di magnesio si ottiene trattando soluzioni di cloruro di magnesio, solitamente acqua di mare, con calce.
A temperatura ambiente si presenta come un solido bianco inodore. Talvolta l'ossido di magnesio MgO, prodotto di calcinazione della magnesite (MgCO3), viene indicato con il termine magnesia. Calcinando la magnesite tra 300 e 1200 °C (a seconda del tempo di permanenza nel forno di cottura) si ottiene la magnesia leggera, detta anche magnesia caustica, impiegata nei cementi Sorel. A temperature più elevate, tra i 1.200 ed i 1.800 °C si ottiene invece la magnesia pesante, usata per materiali refrattari basici.
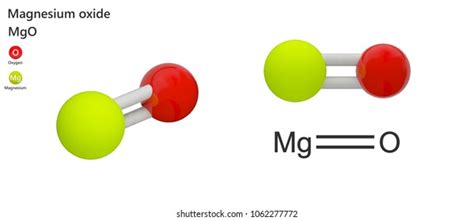
L’ossido di magnesio è una sostanza cristallina bianca. È scarsamente solubile in acqua, ma facilmente solubile negli acidi. L'ossido di magnesio ha numerose proprietà utili nell’industria. Innanzitutto, ha una buona refrattarietà: mantiene la sua durata anche se esposto a temperature elevate. L’ossido di magnesio è anche resistente alla corrosione e ha un’elevata conducibilità termica ma una bassa conducibilità elettrica, quindi può trasferire calore ma non elettricità. L’ossido di magnesio è inoltre caratterizzato da una rapida idratazione a idrossido, che è una base debole.
L’ossido di magnesio è ampiamente utilizzato nell’industria. Viene utilizzato nella produzione di cemento, mattoni, getti, recipienti refrattari e attrezzature di laboratorio. L’ossido di magnesio si trova nei cosmetici, aggiunto a polveri, fondotinta o lozioni. Le sue proprietà di neutralizzazione degli odori sono utilizzate negli antitraspiranti. L’ossido di magnesio è utilizzato anche dagli atleti, in quanto impedisce alle mani di scivolare durante l’arrampicata o l’allenamento con i pesi. L’ossido di magnesio si trova anche nell’industria del riscaldamento per la produzione di riscaldatori a olio, fili riscaldanti e non combustibili o riscaldatori ad accumulo.

Un uso molto importante dell’ossido di magnesio è quello nei mangimi per animali. Come già detto, l’ossido di magnesio è uno dei componenti dei mangimi. La mancanza o la carenza di ossido di magnesio può portare alla tetania dell’erba e a disturbi simili. Viene anche utilizzato per ridurre lo stress negli animali. Gli animali stressati possono causare lotte tra le mandrie, non hanno appetito, sono letargici, crescono più lentamente e sono più suscettibili a malattie e infezioni. Vale la pena ricordare che l’ossido di magnesio è uno dei tanti integratori alimentari con magnesio disponibili sul mercato. Essendo essenziale per la salute umana, è opportuno integrarlo in caso di carenza. L’ossido di magnesio è vitale sia per l’uomo che per gli animali ed è sicuro nella giusta dose.
Per la determinazione del titolo di ossido di magnesio in un minerale, è possibile utilizzare diversi metodi analitici qualitativi. Uno di questi prevede l'uso del Magneson I come reagente. La procedura generale comprende i seguenti passaggi:
Metodo con Magneson I
Reagenti:
- Soluzione satura di Magneson I in alcool etilico assoluto
- KOH (potassio idrossido) in gocce
Procedimento:
- In un beker da 50 mL trasferire 20 mL di campione minerale.
- Aggiungere 1 goccia di soluzione di Magneson I. La soluzione dovrebbe inizialmente assumere una colorazione gialla.
- Addizionare 1 goccia di KOH e mescolare.
- In presenza di magnesio, si formerà dapprima un colore blu che presto si trasformerà in un precipitato dello stesso colore, rimanendo in sospensione nel liquido.
- È consigliabile operare in parallelo una prova in bianco per confronto.
Nota: Per l'esecuzione del test, se si utilizza acqua di rubinetto come campione, il suo contenuto di magnesio, determinato per via complessometrica, è di circa 6 ppm. Il limite di rilevabilità con questo metodo può essere stimato intorno a 1,5 ppm.
Metodo con Giallo Tiazolo G
Il composto, noto anche come giallo tiazolo G (CAS n° 1829-00-1), è più sensibile del Magneson I e può identificare fino a 0,3 ppm di Mg.
Procedura:
- A 20 mL di campione minerale si aggiungono 0,5 mL di reattivo (soluzione acquosa allo 0,1% di giallo tiazolo G, stabile per circa due settimane).
- Successivamente, si aggiunge una goccia di KOH mescolando fino a completa dissoluzione.
Sebbene questo metodo trovi impiego anche in analisi quantitative, richiede condizioni operative particolari e attentamente controllate, come limiti di assorbanza specifici, presenza di calcio in eccesso, stabilizzazione del precipitato con un addensante e mantenimento di una temperatura costante.
Metodo con Chinalizarina
Questo metodo utilizza una soluzione alcolica satura di chinalizarina (CAS n° 81-61-8), un noto colorante antrachinonico.
Reagenti:
- Soluzione alcoolica satura di chinalizarina
- KOH solido (o 1M)
Esecuzione del test:
- In un piccolo beker introdurre 5 mL di campione minerale.
- Aggiungere 2 mL di reattivo chinalizarina e mescolare, attendendo 1 minuto.
- Poi, sotto costante agitazione, dosare la soluzione di KOH goccia a goccia fino ad ottenere una colorazione gialla.
- In presenza di Mg si osserva una colorazione bruna con separazione di fiocchi dello stesso colore.
La sensibilità di questa reazione dipende dal tenore di iodio libero (evidenziato dalla colorazione gialla). Se la colorazione gialla appare debole, può essere ravvivata con 1-2 gocce del reattivo. Questa reazione è meno sensibile delle precedenti, ma permette di identificare con sicurezza almeno 6 ppm di magnesio, specialmente se il liquido viene osservato a debole ingrandimento al microscopio.
Esecuzione test Magnesio Salifert - Semplice e veloce!
Per quanto riguarda la produzione di ossido di magnesio, un interessante esperimento che permette di produrlo consiste nello scaldare una strisciolina di magnesio al becco Bunsen. L’ossido di magnesio, ottenuto per calcinazione del carbonato di magnesio naturale sopra gli 800°C, si presenta in diverse forme a seconda della temperatura di calcinazione:
- Magnesia caustica: ottenuta per calcinazione tra 300 e 1200 °C, dotata di proprietà idrauliche e contenente fino al 10-15% di carbonato.
- Magnesia bruciata: ottenuta per calcinazione in forni a tino a circa 1600-1700 °C, contenente ossidi di ferro e di manganese, usata per mattoni e rivestimenti refrattari.
- Magnesite fusa: ottenuta al forno elettrico fino ad incipiente fusione, usata come materiale altamente refrattario e contenente il 94-96% di MgO.
Il cloruro di magnesio, un altro composto correlato, si ricava in quantità rilevante dai giacimenti salini di Stassfurt, o può essere preparato in laboratorio per reazione del cloro a caldo sopra una mescolanza di ossido e carbone. Il magnesio pidolato è il sale di magnesio dell'acido pidolico (PCA), anche noto come acido piroglutammico. Il solfato di magnesio, o sale inglese o sale amaro (sale di Epsom), viene utilizzato in dosaggi bassi come lassativo, in dosi elevate come purgante energico in caso di scompenso cardiaco o uremie.
In sintesi, l'ossido di magnesio è un composto versatile con numerose applicazioni industriali e mediche, la cui determinazione nei minerali può essere effettuata tramite specifici test colorimetrici.