Gli amminoacidi sono composti organici essenziali per la vita, costituendo i mattoni fondamentali delle proteine. La loro struttura chimica, caratterizzata dalla presenza di un gruppo amminico e un gruppo carbossilico, conferisce loro proprietà uniche e una vasta gamma di funzioni biologiche.
Struttura e caratteristiche degli amminoacidi
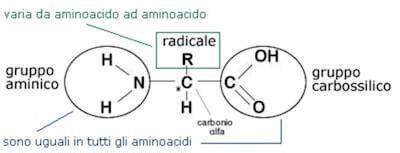
Gli amminoacidi sono composti organici quaternari formati da carbonio, ossigeno, idrogeno e azoto; alcuni di essi contengono anche atomi di zolfo, un elemento che ha una rilevante importanza dal punto di vista nutrizionale. L'azoto è presente in forma di gruppo amminico che, insieme al gruppo carbossilico, costituisce la caratteristica comune di tutti gli amminoacidi. La specificità del singolo amminoacido è determinata invece dalla natura chimica del gruppo laterale, che viene indicato con la lettera R.
Gli amminoacidi cristallizzano in soluzione acquosa neutra in forma di ioni bipolari (zwitterioni) e sono caratterizzati da un'elevata costante dielettrica e da elevati momenti bipolari. Tutti gli amminoacidi, con la sola eccezione della glicina, possiedono almeno un atomo di carbonio asimmetrico, cioè legato a quattro gruppi diversi, e sono pertanto dotati di attività ottica. Questo significa che quando vengono esaminati in un polarimetro, essi sono in grado di far ruotare il piano della luce polarizzata verso destra o verso sinistra. La stereochimica degli amminoacidi, tuttavia, viene espressa in termini di configurazione assoluta, avendo come termine di riferimento la L-gliceraldeide, piuttosto che di rotazione specifica. Tutti gli amminoacidi stereochimicamente correlati con la L-gliceraldeide sono indicati con la lettera L, mentre quelli correlati con la D-gliceraldeide sono indicati con la lettera D, senza tener conto della direzione di rotazione del piano della luce polarizzata. Gli amminoacidi naturali e, in particolare, quelli che costituiscono le proteine, appartengono tutti alla serie L.
Già da tempo però aminoacidi della serie D sono stati riscontrati in natura, in particolare nei microrganismi, in alcuni insetti, negli invertebrati marini, nelle piante superiori e, ultimamente, anche nei mammiferi. Gli amminoacidi della serie D possono anche formarsi in seguito alla cottura degli alimenti o a trattamenti tecnologici.
La catena laterale di un amminoacido viene convenzionalmente chiamata gruppo R, questo perché in chimica organica il sostituente indica un generico sostituente che è di natura alchilica o che inizia come tale e che poi può contenere altri gruppi funzionali. In funzione delle proprietà chimiche del gruppo R, un amminoacido viene classificato come acido, basico, idrofilo o idrofobo. La catena laterale assume un ruolo fondamentale nelle interazioni tra amminoacidi.
Funzioni degli amminoacidi
Gli amminoacidi svolgono nell'organismo tre diverse funzioni. Innanzitutto costituiscono gli elementi di base delle proteine, nelle quali sono uniti l'uno con l'altro mediante legami peptidici: le diverse migliaia di proteine esistenti sono dovute proprio alla diversa sequenza dei singoli amminoacidi. Essi inoltre, come tali o in forme da essi derivate, danno origine ad alcuni ormoni e mediatori chimici, oltre che ad altre molecole di importanza biologica. Gli amminoacidi rappresentano, infine, un'essenziale fonte di energia per l'organismo.
La funzione principale degli L-α-amminoacidi è quella di essere i costituenti fondamentali delle proteine. La struttura primaria di una proteina, ovvero la sua struttura lineare, è composta da una catena di amminoacidi uniti da legami covalenti. Alcuni amminoacidi non proteinogenici sembrano essere inclusi nelle strutture proteiche. Ciò accade perché gli L-α-amminoacidi possono venire modificati dopo la loro inclusione nelle proteine. Un esempio è l'idrossiprolina, derivata dalla prolina, che è un componente importante del collagene. Allo stesso modo, in alcune proteine dei procarioti, avviene l'inclusione degli D-α-amminoacidi.
Gli amminoacidi non proteinogenici si trovano spesso come intermedi delle vie metaboliche; ad esempio la carnitina, un amminoacido il cui gruppo amminico è derivato dall'ammonio, è usata nel trasporto dei lipidi. L'ornitina e la citrullina sono intermedi del ciclo dell'urea.
Classificazione degli amminoacidi
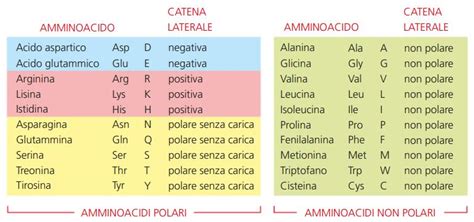
Sono stati proposti vari tipi di classificazione degli amminoacidi, tutti basati sulla natura dei gruppi R. Il criterio più diffuso è quello basato sulla polarità dei gruppi laterali, misurata a pH 6,0-7,0, cioè al normale pH intracellulare; in base a tale criterio, si possono individuare quattro classi principali di amminoacidi: non polari o idrofobici, polari ma privi di carica, carichi positivamente, carichi negativamente.
Gli amminoacidi possono essere classificati in base al gruppo radicale che li differenzia. Sono amminoacidi dotati di catene laterali idrofile e con carica positiva l'arginina, l'istidina e la lisina, mentre sono dotati di carica negativa l'acido aspartico e l'acido glutammico. Presentano catene laterali idrofile polari ma prive di carica la serina, la treonina, l'asparagina, la glutammina e la tirosina, mentre sono classificati a catene laterali apolari idrofobiche l'alanina, la isoleucina, la leucina, la metionina, la fenilalanina, il triptofano e la valina. Rientrano nei casi speciali la cisteina, la glicina e la prolina, in quanto la catena laterale della glicina è formata da un solo atomo di idrogeno, il gruppo radicale della cisteina presenta un gruppo terminale -SH, che le consente di reagire con la catena laterale di un'altra unità di cisteina, formando un legame covalente chiamato ponte disolfuro. Per quanto riguarda la prolina, essa presenta un gruppo amminico modificato, privo di atomi di idrogeno, che le consente di formare una struttura ad anello.
Amminoacidi essenziali
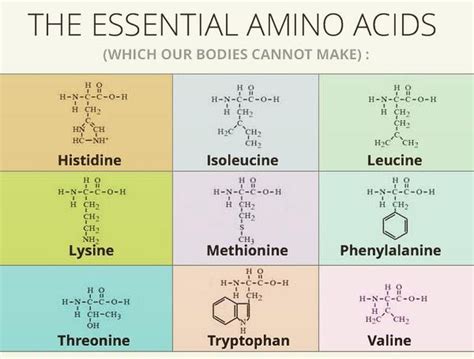
Si definiscono 'essenziali' quegli amminoacidi, indispensabili alle normali funzioni dell'organismo, che esso non è in grado di sintetizzare e che devono quindi essere presenti nella dieta. Il termine essenziale ha un significato unicamente nutrizionale, in quanto per la sintesi delle proteine sono ovviamente necessari tutti e 20 gli amminoacidi che le costituiscono. Gli amminoacidi essenziali per i mammiferi sono 9, e precisamente lisina, treonina, metionina, valina, leucina, isoleucina, fenilalanina, triptofano e istidina. In condizioni particolari, come nei neonati prematuri e nei soggetti con danno epatico, diventano essenziali anche altri amminoacidi, per es.
Dei venti amminoacidi proteici, alcuni sono definiti "essenziali". Un amminoacido è definito essenziale se all'interno dell'organismo non sono presenti le strutture (enzimi, proteine di sintesi) necessarie a biosintetizzarlo; è perciò necessario che questo amminoacido venga introdotto con la dieta. Gli amminoacidi essenziali sono la lisina, la leucina, l'isoleucina, la metionina, la fenilalanina, la treonina, il triptofano, la valina e l'istidina. Riguardo all'istidina, è importante precisarne l'essenzialità: l'istidina è un amminoacido essenziale durante tutta la vita, ma durante l'età adulta il fabbisogno non è molto rilevante, poiché l'organismo riesce a conservarla in modo particolarmente efficiente, riducendone la richiesta biologica.
Esistono poi amminoacidi condizionatamente essenziali, ossia che devono essere assunti con la dieta solo in alcuni periodi della vita o a causa di alcune patologie. Di questo gruppo fanno parte l'arginina, la tirosina e la cisteina.
Gli amminoacidi essenziali sono indispensabili per la sintesi proteica (i cosiddetti AA proteo sintetici), contribuendo ad una funzione plastica, come ad esempio possiamo riscontrare nella sintesi della carnitina, che avviene solo se metionina e lisina sono disponibili nelle quantità necessarie; ricordiamo che metionina e lisina fanno per l’appunto parte dei 9 aminoacidi essenziali. Gli EAA possono intervenire nella produzione energetica, nella risposta immunitaria, nella sintesi di ormoni e vitamine, nella trasmissione degli impulsi nervosi, e come catalizzatori in moltissimi processi metabolici.
Amminoacidi non essenziali
I 12 amminoacidi non essenziali sono sintetizzati dall'organismo "ex novo" a partire da sostanze quaternarie più semplici; essi sono alanina, arginina, acido aspartico, cisteina, acido glutammico, glicina, prolina, serina, tirosina, asparagina, istidina, glutammina.
Due di tali amminoacidi, l'arginina e l'istidina, da alcuni autori sono ritenuti essenziali, ma solo durante la fase della crescita, anche se altri autori li ritengono essenziali anche nell'adulto. Sono considerati semi-essenziali la cisteina e la tirosina, perché l'organismo li può sintetizzare a partire da altri amminoacidi (metionina e fenilalanina).
Ruolo degli amminoacidi nell'organismo e nell'alimentazione
Gli amminoacidi costituiscono il 20% del corpo umano e sono elementi critici per la vita. La loro presenza è fondamentale per garantire le funzioni muscolari, cerebrali ed ematiche. Le strutture carbossiliche degli amminoacidi vengono riutilizzate nel fegato e tornano ai muscoli sotto forma di glucosio. Le proteine, scisse in amminoacidi, vengono dunque utilizzate a scopo energetico tramite la conversione in molecole glucidiche o direttamente in intermedi del ciclo di Krebs.
Gli amminoacidi sono i costituenti base delle proteine e rappresentano le "tessere" o i "mattoni", che assemblandosi in vario modo costituiscono le diverse proteine che andranno a formare pelle, muscoli, tendini, capelli, unghie, ossa, ecc. Anche la struttura portante delle singole cellule, chiamata citoscheletro, è formata da proteine, ne determina la forma, che è variabile, e ne consente il movimento. Nell'organismo le proteine svolgono svariate funzioni, da quella enzimatica, indispensabile per la scomposizione e la trasformazione di altre molecole, a quella energetica, al pari dei glucidi e dei lipidi, ma con una importanza secondaria, come già detto, rispetto alla funzione strutturale, in quanto la funzione energetica è attivata solo in caso di carenza di altre fonti, e solo in condizione di necessità, anche per la sua minore efficienza dal costo energetico rilevante rispetto all'energia fornita da glucidi e lipidi.
Gli alimenti di origine animale, come carne, uova, latticini, pesce, contengono tutti gli amminoacidi essenziali; quelli di origine vegetale hanno generalmente una composizione non completa: i cereali, come la pasta, mancano di alcuni amminoacidi, altrettanto ma in grado minore anche i legumi, la frutta a guscio e i semi oleosi. Una buona strategia consiste perciò nell'associare cereali e legumi, come ad esempio pasta e fagioli, pasta e ceci, nelle classiche ricette della Dieta Mediterranea, oppure mais e fagioli, soia e riso, per raggiungere una completezza nutrizionale di tutti gli amminoacidi essenziali.
Produzione e sintesi degli amminoacidi
Esistono due tipi di processi per la produzione su larga scala di amminoacidi, i processi chimici e quelli biotecnologici. Con i primi si ottiene il prodotto racemico, cioè L- e D-amminoacidi in uguale proporzione, ed è quindi necessario un ulteriore trattamento per isolare la forma L, cioè quella biologicamente attiva. Con i secondi invece si ottiene direttamente la forma L e, grazie alla notevole semplificazione del processo, sono possibili rese molto elevate e un cospicuo abbattimento dei costi. Tra i processi biotecnologici possono essere distinti i processi fermentativi e quelli di biotrasformazione. Negli ultimi anni la produttività di alcuni ceppi è stata migliorata grazie all'impiego di tecniche di ingegneria genetica.
Nei processi di biotrasformazione invece una sostanza A (per es., un precursore o un intermedio) viene trasformata nella sostanza B mediante l'uso di un biocatalizzatore (enzima) di origine microbica o purificato da cellule animali o vegetali. I biocatalizzatori hanno il vantaggio, rispetto ai catalizzatori chimici, di essere fortemente specifici o stereospecifici. Spesso vengono impiegati enzimi in soluzione o enzimi immobilizzati, che rimangono attivi per tempi molto lunghi.
Insegnamento di Processi chimici innovativi
La produzione commerciale di amminoacidi di solito si basa su batteri mutanti che producono in eccesso i singoli amminoacidi utilizzando il glucosio come fonte di carbonio. Alcuni amminoacidi sono prodotti da conversioni enzimatiche di intermedi sintetici. In laboratorio, la maggior parte degli amminoacidi non proteinogenici viene prodotta attraverso sintesi di Strecker o amminazione riduttiva su derivati della condensazione di Claisen. Un'ulteriore via di sintesi è la sintesi asimmetrica, mediante reattivo di Corey, su α-chetoesteri.
Amminoacidi e sport
Gli amminoacidi essenziali (EAA) sono sostanze particolarmente ricercate in ambito sportivo grazie alle loro importanti funzioni muscolare, sono infatti necessari ad esempio per costruire nuovi tessuti, favorire la riparazione muscolare e risultano essere utili contro la stanchezza e lo stress. Il recupero muscolare, che è uno dei fattori necessari affinché il nostro fisico possa tollerare al meglio allenamenti via via più intensi, evitando lesioni tissutali ed eccessivi dolori nei giorni che seguono il training, è legato alla disponibilità di questi amminoacidi, poi chè essi svolgono funzioni chiave nei sistemi di regolazione della sintesi proteica.
Uno dei ruoli principali degli EAA (aminoacidi essenziali) negli sport di forza, riguarda proprio la loro azione sulla sintesi proteica. È utile sapere che, per fare in modo che questo processo di sintesi avvenga, è necessario che siano presenti contemporaneamente tutti gli aminoacidi necessari per la costruzione della nuova proteina muscolare. Quindi, come abbiamo già visto, si definisce ‘amminoacido limitante’ quell'amminoacido essenziale la cui carenza o insufficienza limita la sintesi di nuove proteine.
Gli aminoacidi ramificati (BCAA) trovano grande applicazione in ambito sportivo, perché coinvolti nella prevenzione e protezione dei muscoli prima, nella fase di lavoro e superlavoro muscolare durante lo sforzo, e di ricostruzione e recupero dopo. La sostanziale differenza con gli altri tipi di aminoacidi essenziali sta nella fase di metabolizzazione: mentre gli altri, infatti, vengono sintetizzati già nell’intestino, i ramificati proseguono il loro “percorso” fino ai muscoli andando a sostenere la funzione plastica di ricostruzione del tessuto e della massa muscolare.

tags: #classificazione #di #rose #degli #aminoacidi