Le proteine occupano un ruolo primario nel mondo biologico: senza di esse non sarebbe possibile alcuna forma di vita.
In chimica, le proteine (o protidi) sono macromolecole biologiche costituite da catene di amminoacidi legati uno all'altro da un legame peptidico (ovvero un legame tra il gruppo amminico di un amminoacido e il gruppo carbossilico dell'altro amminoacido creato attraverso una reazione di condensazione con perdita di una molecola d'acqua).
La loro composizione elementare è abbastanza costante (carbonio, idrogeno e azoto).
Gli amminoacidi si legano tra loro tramite legami ammidici, formando prima dipeptidi e poi catene sempre più lunghe, fino a generare polipeptidi e vere e proprie proteine.
Livelli di Organizzazione delle Proteine
Le proteine hanno una struttura tridimensionale molto complessa a cui è associata sempre una funzione biologica.
La struttura primaria è definita dalla sequenza ordinata degli amminoacidi e rappresenta l'informazione di base della proteina, direttamente codificata dal DNA.
Una catena lineare di residui amminoacidici è chiamata "polipeptide" (ovvero una catena di più amminoacidi legati da legami peptidici).
Se la molecola è costituita da poche unità di amminoacidi (in genere non più di 10) viene definita un "oligopeptide". Molecole con più di 10 unità sono dette "polipeptidi".
La sequenza degli aminoacidi in una proteina è definita dalla sequenza presente in un gene, la quale è codificata nel codice genetico.
Proteine che contengono lo stesso tipo e numero di amminoacidi possono differire dall'ordine in cui questi sono situati nella struttura della molecola.
Tale aspetto è molto importante perché una minima variazione nella sequenza degli amminoacidi di una proteina (cioè nell'ordine con cui i vari tipi di amminoacidi si susseguono) può portare a variazioni nella struttura tridimensionale della macromolecola che possono rendere la proteina non funzionale.
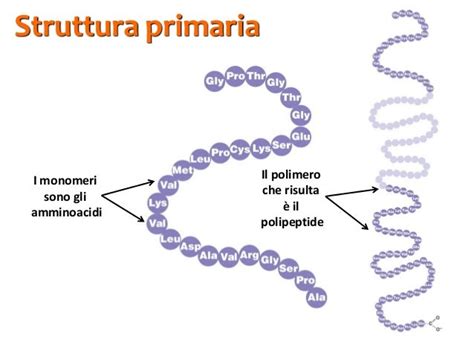
La struttura secondaria (α-elica e β-foglietto) è stabilizzata da legami a idrogeno ed è sensibile a calore e agenti chimici, che possono provocare denaturazione.
L'α-elica è la conformazione più comune riscontrabile nelle proteine, particolarmente presente nei recettori cellulari, dov'è immersa nella membrana plasmatica della cellula, spesso con più α-eliche per singola proteina (unite da catene polipeptidiche ad U).
L'elica è una delle conformazioni più favorevoli perché naturalmente riduce al minimo l'energia libera, può essere sinistrorsa o destrorsa.
Fu scoperta per la prima volta nell'α-cheratina negli anni Sessanta.
L'α-elica si forma quando una catena polipeptidica si ripiega su se stessa con formazione di legami idrogeno tra un legame peptidico e il quarto successivo, in particolare tra il gruppo chetonico C=O dell'uno e il gruppo N-H dell'altro, e il legame è tra O e H.
Tutti i gruppi amminici di un'elica sono rivolti verso l'N-terminale della proteina, tutti quelli chetonici verso il C-terminale, così l'elica assume parziale carica positiva all'N-terminale e parziale carica negativa al C-terminale.
L'elica che si forma ha un giro completo ogni 3,6 amminoacidi e la distanza media tra questi è 0,54 nm.
In alcune proteine due o tre α-eliche si avvolgono l'una intorno all'altra formando il coiled coil.
Generalmente questa conformazione è assunta quando ciascuna elica ha la maggior parte delle catene laterali di amminoacidi idrofobici da un lato, in questo modo, sfruttando le attrazioni idrofobiche, le eliche possono avvolgersi una intorno all'altra.
Nella struttura a β-foglietto si possono formare dei legami a idrogeno tra amminoacidi appartenenti a catene polipeptidiche differenti ma tra loro parallele oppure tra amminoacidi di una stessa proteina anche numericamente lontani tra loro ma che scorrono in direzioni antiparallele.
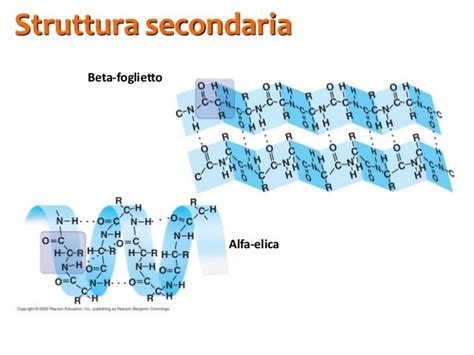
La struttura terziaria deriva dal ripiegamento complessivo della catena e dipende soprattutto dai legami disolfuro.
Le proteine assumono la struttura terziaria quando la loro catena, pur sempre flessibile nonostante la piegatura della struttura secondaria, si ripiega in modo da originare una contorta disposizione tridimensionale a forma di corpo solido.
Una porzione di proteina che si ripiega indipendentemente dal resto della catena polipeptidica è detta dominio proteico ed una proteina può averne anche più di uno.
Tra gli atomi di una proteina si stabiliscono interazioni dette legami, che possono essere covalenti o non covalenti.
I legami non covalenti, presi singolarmente, sono sempre più deboli dei covalenti nell'ordine di decine o centinaia di volte, tuttavia il loro numero all'interno di una proteina li rende fondamentali per comprenderne il ripiegamento.
A queste interazioni si deve aggiungere la tendenza dei gruppi di amminoacidi idrofobici (fenilalanina, leucina, isoleucina, triptofano, valina, cisteina, metionina, prolina, alanina e glicina) ad avvicinarsi e unirsi tra loro, formando delle tasche idrofobiche lontane dalla rete di legami idrogeno che deve essere immaginata sempre presente all'interno di un ambiente acquoso tra le molecole d'acqua.
Generalmente i gruppi di amminoacidi idrofobici sono quasi sempre posti all'interno della proteina, dal momento che questa si trova tipicamente in un ambiente acquoso, mentre i suoi amminoacidi idrofili, polari e con carica, saranno tendenzialmente all'esterno.
È stato possibile scoprire questa peculiarità delle proteine effettuando esperimenti di denaturazione (tramite solventi come l'urea) e rinaturazione di proteine in vitro.
Si è notato che alcune proteine, una volta denaturate e rimosso il solvente si ripiegavano autonomamente.
Tuttavia, non tutte le proteine una volta denaturate possono ripiegarsi spontaneamente nella loro conformazione originaria.
La conformazione di una proteina, benché sia normalmente la più stabile possibile per la sequenza dei suoi amminoacidi, non è immutabile, e subisce piccole modificazioni dovute all'interazione con ligandi o altre proteine.
Questa caratteristica è alla base della funzionalità della maggior parte delle proteine.
La conformazione di una proteina può essere notevolmente aiutata ed affinata dagli chaperoni, delle proteine che si legano alle catene parzialmente ripiegate e le assistono sino a raggiungere la conformazione corretta.
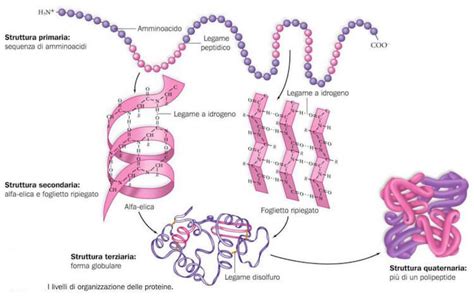
La struttura quaternaria, invece, compete solo alle proteine formate da due o più subunità.
Aggregati specifici di due o più catene polipeptidiche ripiegate, o subunità.
Proteine e associazione tra subunità di struttura molto diversa (interazioni eterotipiche).
In entrambi i casi si ha la formazione di proteine mulitmeriche.
Funzioni delle Proteine
Le proteine svolgono una vasta gamma di funzioni all'interno degli organismi viventi, tra cui la catalisi delle reazioni metaboliche, funzione di sintesi come replicazione del DNA, la risposta agli stimoli e il trasporto di molecole da un luogo ad un altro.
In analogia con altre macromolecole biologiche come i polisaccaridi e gli acidi nucleici, le proteine costituiscono una parte essenziale degli organismi viventi e partecipano praticamente in ogni processo che avviene all'interno delle cellule.
Molte fanno parte della categoria degli enzimi, la cui funzione è catalizzare le reazioni biochimiche vitali per il metabolismo degli organismi.
Altre sono fondamentali per la trasmissione di segnali inter ed intracellulari, nella risposta immunitaria, per l'adesione cellulare e per il ciclo cellulare.
Le proteine sono elementi necessari anche nell'alimentazione degli animali, dal momento che essi non possono sintetizzare tutti gli amminoacidi di cui hanno bisogno e devono ottenere quelli essenziali attraverso il cibo.
Tra le altre funzioni delle proteine rientrano la regolazione dell'espressione dei geni, la duplicazione, trascrizione e traduzione del DNA, la regolazione delle reazioni metaboliche, la generazione e la ricezione degli impulsi nervosi.
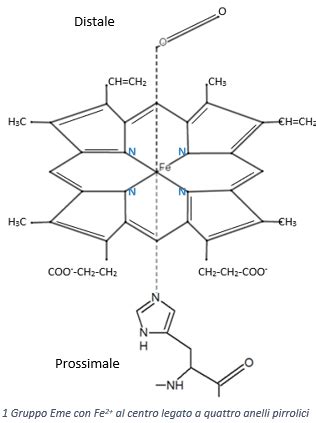
Le proteine di trasporto si legano a sostanze poco idrosolubili e ne consentono il trasporto nei liquidi corporei.
Classificazione delle Proteine
La classificazione può essere dunque fatta in base alla composizione chimica, alla configurazione molecolare o alla solubilità.
Si distinguono così proteine semplici (costituite da soli amminoacidi) e proteine coniugate (costituite da una proteina semplice e da un gruppo prostetico di natura non proteica).
Tra le proteine semplici vi sono le proteine fibrose, generalmente insolubili nei solventi acquosi ed a volte inattaccabili dagli enzimi proteolitici, come ad esempio: il collagene (costituente essenziale del tessuto connettivo), l'elastina (componente principale delle fibre elastiche e delle pareti vasali), la cheratina (componente essenziale dell'epidermide).
Inoltre, sempre tra quelle semplici vi sono le proteine globulari, le albumine (assai diffuse nel mondo animale), le globuline (insolubili in acqua, si trovano nel sangue, nel muscolo, nei tessuti in genere e nei semi) e le prolamine (caratteristiche del mondo vegetale).
Proteine fibrose sono caratterizzate da una forma filamentosa, allungata.
Proteine globulari presentano una conformazione compatta e sferica, tipica delle proteine con funzione enzimatica o regolatoria.
Studio e Modifica delle Proteine
Le proteine possono essere purificate da altri componenti cellulari utilizzando una varietà di tecniche come l'ultracentrifugazione, la precipitazione, l'elettroforesi e la cromatografia; l'avvento dell'ingegneria genetica ha reso possibile una serie di metodi per facilitare tale purificazione.
I metodi comunemente usati per studiare la struttura e la funzione delle proteine includono immunoistochimica, la mutagenesi sito specifica, la cristallografia a raggi X, la risonanza magnetica nucleare.
Poco dopo o anche durante la sintesi proteica, i residui di una proteina vengono spesso modificati chimicamente mediante la modificazione post traduzionale, che se presente altera le proprietà fisiche e chimiche, la piegatura, la stabilità, l'attività e, in ultima analisi, la funzione della proteina.
Cristallografia a raggi X | Animazione di biologia strutturale per esami CSIR NET e scienze della...
La formazione di copie duplicate di geni e l'alterazione della funzione di una proteina nel corso dell'evoluzione hanno portato alla formazione delle circa 500 famiglie proteiche identificate.
All'interno di una famiglia, sebbene ciascuna proteina svolga una funzione leggermente diversa dall'altra, la sequenza di amminoacidi, in particolare presso i siti catalitici e in regioni conservate, è quasi identica.
Si può quindi affermare che nel corso dell'evoluzione all'interno di una famiglia proteica si è conservata più la conformazione tridimensionale che non la sequenza degli amminoacidi.
Generalmente, quando almeno un quarto della sequenza amminoacidica di due proteine corrisponde, esse hanno la stessa struttura generale.
Due proteine diverse appartenenti a una stessa famiglia e dalla funzione simile sono dette "paraloghe", mentre la stessa proteina in due organismi diversi (per esempio uomo e topo) è detta "ortologa".
Esempi Specifici di Proteine
Rappresentazione schematica della mioglobina. Quest'omologo proteico dell'emoglobina lega l'ossigeno nei muscoli.
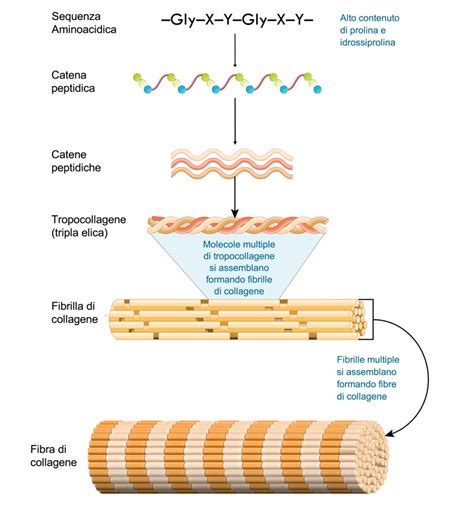
Il collagene è la proteina più abbondante in natura ed è essenziale per la resistenza e l'elasticità di tessuti come ossa, tendini e pelle.
La sua struttura a tripla elica, ricca di glicina e prolina, gli conferisce caratteristiche meccaniche uniche.
Una delle proprietà più curiose del collagene è la sua semplicità costitutiva: è formato per circa il 30% da prolina e per circa il 30% da glicina; gli altri 18 amminoacidi si devono spartire solamente il restante 40% della struttura proteica.
La prolina è un amminoacido ciclico in cui il gruppo R si lega all'azoto α-amminico e ciò conferisce una certa rigidità.La struttura finale è una catena ripetitiva avente la forma di un'elica; all'interno della catena di collageno, sono assenti legami a idrogeno.
La coagulazione richiede almeno trenta enzimi specializzati.
Dopo il coagulo si deve proseguire con la riparazione del tessuto; le cellule vicine alla ferita producono anche collagene.
Per far ciò, per prima cosa viene indotta l'espressione di un gene cioè entrano in funzione organismi che partendo dall'informazione di un gene, sono in grado di produrre la proteina (l'informazione genetica viene trascritta sull'mRNA il quale esce dal nucleo e raggiunge i ribosomi nel citoplasma dove l'informazione genetica viene tradotta in proteina).
Successivamente, per azione di altri enzimi, si verificano altre modificazioni che consistono nella glicosidazione dei gruppi ossidrili di prolina e lisina (all'ossigeno dell'OH si lega uno zucchero); tali enzimi si trovano in zone diverse dal lume perciò, la proteina, mentre subisce le modificazioni, migra all'interno del reticolo endoplasmatico per finire in sacche (vescicole) che si richiudono su se stesse e si staccano dal reticolo: al loro interno è contenuto il monomero del pro-collagene glicosidato; quest'ultimo raggiunge l'apparato del Golgi dove particolari enzimi riconoscono la cisteina presente nella parte carbossi terminale del pro-collagene glicosidato e fanno sì che le diverse catene si avvicinino tra loro e formino dei ponti disolfuro: si ottengono così tre catene di pro-collagene glicosidato legate tra loro ed è questo il punto di partenza del quale le tre catene, compenetrando, poi, spontaneamente, danno origine alla tripla elica.