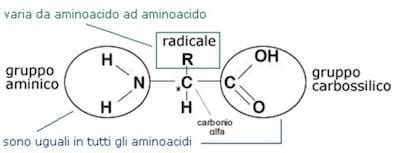
Gli amminoacidi sono i mattoni fondamentali delle proteine, molecole biologiche essenziali che svolgono innumerevoli funzioni nell'organismo umano. La loro struttura chimica, caratterizzata dalla presenza di un gruppo amminico (-NH₂) e un gruppo carbossilico (-COOH) legati a un atomo di carbonio centrale (chiamato carbonio alfa o Cα), li rende particolarmente versatili. Tuttavia, non tutti gli amminoacidi sono uguali: la loro diversità risiede principalmente nella catena laterale, indicata con la lettera "R", che conferisce a ciascuno proprietà uniche.
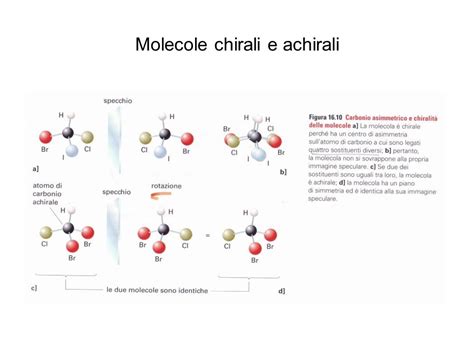
Un aspetto cruciale della chimica degli amminoacidi riguarda la loro chiralità. La chiralità, un concetto fondamentale nella stereochimica, si riferisce alla proprietà di un oggetto (in questo caso, una molecola) di non essere sovrapponibile alla propria immagine speculare. Due molecole che sono immagini speculari non sovrapponibili l'una dell'altra sono chiamate enantiomeri. Questa proprietà è analoga a quella delle nostre mani: la destra è l'immagine speculare della sinistra, ma non sono identiche. Nella maggior parte dei casi, il carbonio alfa di un amminoacido è legato a quattro gruppi differenti (il gruppo amminico, il gruppo carbossilico, un atomo di idrogeno e la catena laterale R), rendendolo un centro stereogenico e la molecola chirale.
Esiste però un'eccezione importante: la glicina. La glicina è l'unico amminoacido che non possiede un centro stereogenico sul carbonio alfa, poiché questo è legato a due atomi di idrogeno. Di conseguenza, la glicina è un amminoacido achirale, ovvero non presenta la proprietà della chiralità. Questo la distingue da tutti gli altri 20 amminoacidi comunemente presenti nelle proteine, noti come amminoacidi proteinogenici, che sono quasi tutti chirali.
La Struttura e le Proprietà degli Amminoacidi
Gli amminoacidi sono composti organici formati da carbonio (C), idrogeno (H), ossigeno (O) e azoto (N). La loro struttura generale è NH₂-CHR-COOH. Il carbonio alfa (Cα) è il centro della molecola, legato a un gruppo amminico (NH₂), un gruppo carbossilico (COOH), un atomo di idrogeno (H) e la catena laterale (R).
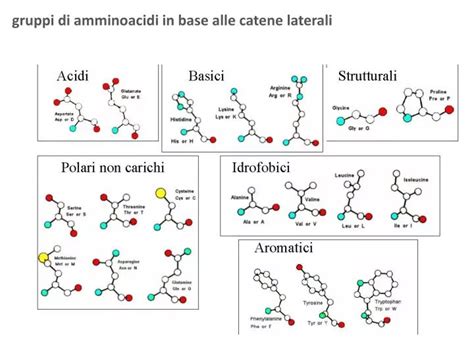
La natura del gruppo R determina le proprietà chimiche e fisiche dell'amminoacido. Le catene laterali possono essere:
- Apolari: Costituite principalmente da idrocarburi, rendono l'amminoacido idrofobico (es. alanina, valina, leucina, isoleucina, metionina, fenilalanina, triptofano, prolina).
- Polari: Contengono gruppi funzionali che possono formare legami idrogeno con l'acqua, rendendo l'amminoacido idrofilo (es. serina, treonina, cisteina, tirosina, asparagina, glutammina).
- Acidi: Possiedono un gruppo carbossilico aggiuntivo nella catena laterale, conferendo una carica negativa a pH fisiologico (es. acido aspartico, acido glutammico).
- Basici: Contengono gruppi amminici aggiuntivi nella catena laterale, conferendo una carica positiva a pH fisiologico (es. lisina, arginina, istidina).
Una proprietà importante degli amminoacidi è quella di essere molecole anfotere, ovvero possono comportarsi sia come acidi che come basi in soluzione acquosa. Questo è dovuto alla presenza simultanea del gruppo carbossilico (acido) e del gruppo amminico (basico). A pH fisiologico, molti amminoacidi si trovano nella forma zwitterionica, con una carica positiva sul gruppo amminico e una carica negativa sul gruppo carbossilico, risultando elettricamente neutri nel complesso.
La Chiralità e la sua Importanza
Come accennato, la maggior parte degli amminoacidi proteinogenici sono chirali a causa della presenza di un centro stereogenico sul carbonio alfa. Le due forme enantiomeriche di un amminoacido sono indicate come L e D. Nella quasi totalità degli organismi biologici, solo gli amminoacidi della serie L vengono utilizzati per la sintesi proteica. Questa "preferenza" per una specifica configurazione spaziale, nota come omichiralità, è fondamentale per la costruzione di proteine con strutture tridimensionali definite e funzionali.
La chiralità delle molecole biologiche, inclusi gli amminoacidi, ha profonde implicazioni. Ad esempio, nel campo farmaceutico, i due enantiomeri di un farmaco possono avere attività biologiche molto diverse, o addirittura opposte. Un esempio storico è la talidomide, dove un enantiomero era un efficace sedativo, mentre l'altro causava gravi malformazioni fetali.
Amminoacidi Non Chirali: L'Eccezione della Glicina
La glicina rappresenta l'unica eccezione tra gli amminoacidi proteinogenici in termini di chiralità. La sua struttura chimica è H₂N-CH₂-COOH. Il carbonio alfa è legato a due atomi di idrogeno, il gruppo amminico e il gruppo carbossilico. Poiché due dei quattro sostituenti sono identici, la glicina non possiede un centro stereogenico ed è quindi achirale.
Questa sua particolare caratteristica la rende unica e le conferisce proprietà specifiche. Ad esempio, la sua piccola dimensione e la mancanza di chiralità le permettono di inserirsi in regioni dove altri amminoacidi chirali potrebbero creare impedimenti sterici. La glicina è spesso trovata nelle regioni flessibili delle proteine, contribuendo alla loro mobilità.
Ruoli e Funzioni degli Amminoacidi
Gli amminoacidi non sono solo i costituenti delle proteine, ma svolgono anche molte altre funzioni vitali:
- Sintesi Proteica: Sono i monomeri che, legati tramite legami peptidici, formano le proteine, essenziali per la struttura, la funzione e la regolazione dei tessuti e degli organi del corpo.
- Precursori di Molecole Biologicamente Attive: Alcuni amminoacidi sono precursori di neurotrasmettitori (es. triptofano per la serotonina, tirosina per la dopamina), ormoni, enzimi e altre molecole fondamentali.
- Metabolismo Energetico: Possono essere catabolizzati per produrre energia, soprattutto in condizioni di digiuno o esercizio fisico prolungato.
- Ruoli Specifici: Alcuni amminoacidi hanno funzioni specializzate. Ad esempio, la cisteina, grazie al suo atomo di zolfo, può formare ponti disolfuro che stabilizzano la struttura tridimensionale delle proteine. La prolina, con la sua catena laterale ciclica, introduce pieghe nelle catene proteiche.
Classificazione degli Amminoacidi
Gli amminoacidi vengono classificati in base a diversi criteri:
- Nutrizionale:
- Essenziali: Non possono essere sintetizzati dall'organismo umano e devono essere assunti con la dieta (es. fenilalanina, isoleucina, istidina, leucina, lisina, metionina, treonina, triptofano, valina).
- Non Essenziali: Possono essere sintetizzati dall'organismo a partire da altri composti (es. alanina, asparagina, acido aspartico, cisteina, acido glutammico, glutammina, glicina, prolina, serina, tirosina).
- Condizionatamente Essenziali: Diventano essenziali in determinate condizioni fisiologiche o patologiche (es. arginina, cisteina, glutammina, tirosina, glicina, prolina, serina).
- Proprietà della Catena Laterale (R): Apolari, polari, acidi, basici.
- Struttura: Chirali e achirali (solo la glicina).
La comprensione della stereochimica degli amminoacidi, inclusa l'eccezione achirale della glicina, è fondamentale per comprendere la struttura e la funzione delle proteine e per molte applicazioni in chimica, biologia e medicina.
LA CHIRALITÀ NEI MONOSACCARIDI
Amminoacidi e Stereochimica: Un Legame Indissolubile
La stereochimica, lo studio della disposizione tridimensionale degli atomi nelle molecole, è intrinsecamente legata alla natura degli amminoacidi. La scoperta delle osservazioni di Pasteur sui cristalli di acido tartarico, che non erano sovrapponibili alla loro immagine speculare, ha aperto la strada alla comprensione della chiralità molecolare. Questa scoperta è stata fondamentale per Giulio Natta e Mario Farina, che hanno dedicato un libro alla stereochimica, riconoscendone l'importanza nella chimica applicata, in particolare nel campo farmaceutico.
La capacità di distinguere e separare enantiomeri, come fece Pasteur con i cristalli di racemato, è cruciale. Tecnologie avanzate permettono oggi l'analisi e la separazione al microscopio, consentendo di individuare gli enantiomeri più isolati e di studiarne le proprietà, come la capacità di ruotare il piano della luce polarizzata. La stereochimica in 3D è quindi di notevole importanza in natura, determinando quasi sempre l'attività chimica di una molecola, specialmente quando interagisce con un enzima.
L'asimmetria sterica, ovvero la chiralità, è un principio guida nella biologia. Gli zuccheri, ad esempio, sono formati da molecole con la medesima chiralità (serie D), e questo è chiaro e fondamentale per la loro funzione biologica. Sebbene la chiralità possa sembrare un concetto astratto, la sua esistenza è di vitale importanza e si estende ben oltre la biosfera, trovando applicazioni in campi come il fotovoltaico, dove la capacità di assorbire luce e convertirla in energia elettrica può dipendere dalla stereochimica dei materiali.
La presenza di stereocentri negli amminoacidi, ad eccezione della glicina, porta alla formazione di molecole chirali. Questi amminoacidi, legati insieme, formano le proteine, la cui struttura tridimensionale è essenziale per la loro funzione. La capacità di una proteina di ripiegarsi correttamente è guidata dalle proprietà chimiche delle catene laterali degli amminoacidi, e qualsiasi impedimento sterico può alterarne la funzionalità.
In sintesi, mentre la glicina si distingue come l'unico amminoacido proteinogenico non chirale, la chiralità gioca un ruolo predominante nella chimica degli amminoacidi e delle proteine. Questa proprietà stereochimica è fondamentale per la vita come la conosciamo, influenzando tutto, dalla struttura delle proteine alla specificità dei farmaci, dimostrando come la disposizione tridimensionale degli atomi sia cruciale per le funzioni biologiche.
tags: #aminoacido #non #chirale