La vitamina C, nota anche come acido ascorbico o acido L-ascorbico, è un nutriente essenziale che gli esseri umani non possono produrre da soli. Ci affidiamo a fonti esterne come frutta e verdura fresca per ottenerlo. La sua storia è strettamente legata alla temuta malattia dello scorbuto, che un tempo rappresentava una delle principali cause di morte tra i marinai. La storia della vitamina C è legata all'età della navigazione e della scoperta, nonché alla temuta malattia dello scorbuto. La scoperta di Lind dei benefici degli agrumi ha stabilito un trattamento praticabile.
Nell'esperimento condotto nel 1747 dal medico navale britannico James Lind, fu confermato che gli agrumi potevano prevenire lo scorbuto. Lind raggruppò dodici marinai affetti da scorbuto in coppie, trattando ogni coppia in modo diverso. I risultati dimostrarono che l'assunzione di arance e limoni permetteva di prevenire l'insorgere dello scorbuto. Di conseguenza, la marina britannica ordinò a tutte le sue navi di trasportare una scorta costante di succo di limoni europei.

Nei secoli successivi, i cibi noti per prevenire lo scorbuto vennero definiti antiscorbutici. Nel 1912, Casimir Funk introdusse il concetto di vitamine come componenti dietetici essenziali, e il "fattore antiscorbutico" fu presto denominato "vitamina C idrosolubile". La vitamina C fu isolata per la prima volta nel 1928 dallo scienziato ungherese Albert Szent-Györgyi. Fu nel 1932 che Szent-Györgyi e Joseph Svirbely conclusero che l'acido esuronico era effettivamente vitamina C, una scoperta confermata quasi contemporaneamente da Charles G. King negli Stati Uniti.
La struttura chimica della vitamina C fu identificata da Walter N. Haworth nel 1933. Lui e Szent-Györgyi proposero che l'acido L-esuronico fosse chiamato acido a-scorbico, a causa della sua funzione antiscorbutica. Oggi, il nostro apporto di vitamina C è solitamente coperto dal consumo di frutta e verdura fresca. La vitamina C è disponibile anche come integratore alimentare e farmaco da banco, oltre a essere utilizzata come conservante alimentare grazie alle sue proprietà antiossidanti.
Struttura Chimica e Proprietà dell'Acido Ascorbico
L'acido ascorbico (C6H8O6) è una molecola che si presenta in forma lineare. La sua struttura è caratterizzata dalla presenza di un anello lattonico e di gruppi ossidrilici. In condizioni fisiologiche e a pH 7, la forma predominante della vitamina C è il monoanione ascorbato, a causa del gruppo -OH enolico legato al C2 dell'anello lattonico, che possiede un pKa di 4,2 rendendolo debolmente acido.
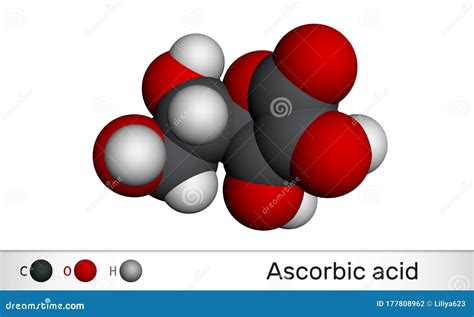
La capacità dell'ascorbato di donare elettroni gli permette di agire come un potente agente antiossidante, eliminando i radicali liberi e riducendo stati di ossidazione elevati del ferro a Fe²⁺. L'acido ascorbico è facilmente ossidato da ossigeno, alcali e alte temperature. Reagisce come un agente riducente relativamente forte e decolora molti coloranti. Forma sali metallici stabili. È incompatibile con ossidanti, coloranti, alcali, ferro e rame.
La degradazione della vitamina C può avvenire attraverso percorsi sia anaerobici che aerobici. La sintesi dell'acido ascorbico avviene industrialmente a partire dal D-glucosio attraverso una serie di reazioni chimiche inframmezzate da fermentazione batterica. Un metodo più semplice prevede l'intervento sequenziale di due specie microbiche: *Erwinia sp.* e *Corynebacterium sp.*
Metodi di Analisi dell'Acido Ascorbico
Per garantire la qualità dei prodotti farmaceutici e rispettare le leggi sull'etichettatura degli alimenti, è necessario determinare il contenuto di vitamina C. La vitamina C viene spesso analizzata mediante titolazione, utilizzando come titolanti il 2,6-diclorofenolindofenolo (DCPIP) o lo iodio. Entrambi questi titolanti reagiscono con l'acido ascorbico in una reazione redox.
Il metodo di titolazione con DCPIP sfrutta il fatto che il DCPIP è rosa salmone, mentre la sua forma ridotta (DCPIPH2) è incolore. La titolazione dello iodio utilizza l'amido come indicatore, che diventa blu-nero in presenza di un eccesso di iodio. La titolazione bivoltametrica misura il potenziale tra due elettrodi polarizzabili; il punto finale si individua quando il potenziale diminuisce bruscamente, indicando che l'acido ascorbico è completamente ossidato.
In alternativa, la vitamina C può essere analizzata con elevata sensibilità mediante polarografia, una tecnica voltammetrica che utilizza un elettrodo a goccia di mercurio (DME). Durante la misurazione polarografica, l'acido ascorbico viene ossidato ad acido deidroascorbico. Il contenuto di acido ascorbico viene determinato mediante aggiunta standard, aggiungendo una soluzione standard di acido ascorbico al campione originale.
La cromatografia ionica (IC) è un altro metodo analitico valido, specialmente quando si devono analizzare anche altri acidi organici. In questo caso, la vitamina C viene determinata come anione ascorbato. Per i succhi contenenti polpa, è necessaria la dialisi in linea per rimuovere le particelle dal campione.
Ruolo Biologico e Applicazioni dell'Acido Ascorbico
L'acido ascorbico è essenziale per la sintesi e il metabolismo della vitamina B9 e della tirosina. Favorisce l'idrossilazione della prolina e della glicina, facilita il metabolismo delle catecolamine, della carnitina e della lisina. Inoltre, l'acido ascorbico favorisce la conversione del colesterolo in acidi biliari, contribuendo a ridurre i livelli di colesterolo nel sangue. Sembra anche poter diminuire la formazione di nitrosammine intestinali e ridurre vari composti ossidanti.
La carenza di vitamina C determina la comparsa dello scorbuto, caratterizzato da insufficiente produzione di collagene e sostanza cementante intercellulare. Questo porta ad alterazioni dei vasi sanguigni con emorragie, rallentamento della cicatrizzazione, gengiviti, gengivorragie e osteoporosi. Nei bambini si osserva anche un arresto della crescita.
Bassi livelli di acido ascorbico, pur sufficienti alla sopravvivenza, sembrano favorire l'aterosclerosi. L'acido ascorbico viene utilizzato per trattare la carenza di vitamina C, lo scorbuto, la guarigione ritardata di ferite e ossa, l'acidificazione delle urine, nella prevenzione e nel trattamento dell'anemia sideropenica e come antiossidante generale.
L'assunzione per via orale di acido ascorbico è generalmente sicura entro i dosaggi raccomandati. Tuttavia, potrebbe essere controindicata in caso di angioplastica, tumori, diabete, malattie ematologiche, calcoli renali, infarto, carenza di G6PD, anemia mediterranea e in fumatori. L'esposizione a questo composto può causare irritazione cutanea, oculare e respiratoria; l'ingestione di grandi quantità può provocare disturbi gastrointestinali e diarrea. In rari casi, l'esposizione può portare alla formazione di calcoli renali di ossalato di calcio.
La vitamina C liposomiale rappresenta una nuova generazione di integratori che, grazie all'incapsulamento in bolle fosfolipidiche, aumenta la capacità di assorbimento dell'acido ascorbico, garantendo un rilascio prolungato e una maggiore biodisponibilità.
Vitamina C e difese immunitarie: cosa dice la scienza
Le informazioni riportate rappresentano indicazioni generali e non sostituiscono in alcun modo il parere medico.