Gli amminoacidi sono molecole organiche essenziali, caratterizzate dalla presenza sia di un gruppo amminico che di un gruppo carbossilico. La loro importanza si estende dalla costituzione delle proteine alla partecipazione in numerosi processi biologici. La biosintesi degli amminoacidi è un processo complesso e vitale, che varia tra i diversi organismi e che permette la produzione sia degli amminoacidi essenziali che di quelli non essenziali.
In biochimica, il termine "amminoacido" si riferisce comunemente agli L-α-amminoacidi, in cui i gruppi amminico e carbossilico sono legati allo stesso atomo di carbonio (α), con una configurazione specifica (L). Questi amminoacidi, noti come proteinogenici, sono i 22 mattoni fondamentali delle proteine. Il legame che unisce questi amminoacidi nelle proteine è definito legame peptidico.
La scoperta del primo amminoacido, l'asparagina, risale al 1806. Successivamente, nel 1810, fu scoperta la cistina, composta da due amminoacidi legati, e solo nel 1884 venne identificata la cisteina. L'ultimo amminoacido proteinogenico scoperto fu la treonina nel 1935.
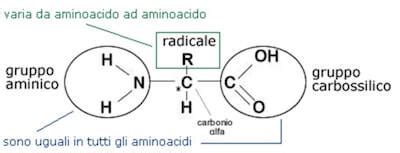
Un amminoacido, per essere tale, deve possedere almeno un gruppo amminico e uno carbossilico. Il carbonio adiacente al gruppo carbossilico è chiamato α, il successivo β, e così via. Se il gruppo amminico è legato al carbonio α, si parla di α-amminoacidi.
A seconda del pH dell'ambiente, i gruppi amminico e carbossilico possono essere neutri o ionizzati. A pH acidi, il gruppo amminico si protona, formando uno ione ammonio. A pH basici, il gruppo carbossilico si deprotona, formando uno ione carbossilato. A pH neutri, molti amminoacidi si trovano in forma zwitterionica, con una carica positiva e una negativa che si bilanciano.
La catena laterale di un amminoacido, detta gruppo R, ne determina le proprietà chimiche (acida, basica, idrofila, idrofoba) e gioca un ruolo cruciale nelle interazioni tra amminoacidi e nel ripiegamento tridimensionale delle proteine.
Quando un atomo di carbonio (in particolare il carbonio α) lega quattro gruppi diversi (gruppo amminico, gruppo carbossilico, un atomo di idrogeno e la catena laterale R), diventa uno stereocentro, dando origine a stereoisomeri L e D. Gli L-α-amminoacidi sono quelli che compongono le proteine degli organismi viventi.
Gli amminoacidi non proteinogenici sono tutti quelli che non partecipano alla sintesi proteica. Molti di essi svolgono ruoli biologici importanti, come intermedi metabolici (es. ornitina, citrullina nel ciclo dell'urea) o neurotrasmettitori (es. GABA, un γ-amminoacido).
La funzione primaria degli L-α-amminoacidi è quella di essere i costituenti delle proteine. Possono subire modifiche post-traduzionali, portando alla formazione di amminoacidi non standard come l'idrossiprolina nel collagene o la D-alanina in alcune proteine batteriche.
Dei 22 amminoacidi proteinogenici, 9 sono essenziali per l'uomo, ovvero non possono essere sintetizzati dall'organismo e devono essere assunti con la dieta: fenilalanina, isoleucina, istidina, leucina, lisina, metionina, treonina, triptofano e valina. Le piante e i procarioti, invece, possiedono vie biosintetiche differenti per produrre questi amminoacidi.
Vie Biosintetiche degli Amminoacidi
La biosintesi degli amminoacidi è un processo fondamentale per la vita, che permette alle cellule di sintetizzare le molecole necessarie per la crescita, la riparazione e il mantenimento dei tessuti. Questi processi sono altamente regolati per soddisfare le esigenze cellulari e ottimizzare l'uso dell'energia.
Le cellule generano amminoacidi a partire da intermedi metabolici derivati da vie metaboliche chiave come la glicolisi, il ciclo dell'acido tricarbossilico (TCA) e la via del pentoso fosfato. L'incorporazione dell'azoto avviene principalmente tramite il glutammato e la glutammina, che fungono da donatori di azoto nelle reazioni di biosintesi.
Fasi Generali della Sintesi degli Amminoacidi
- Formazione della Spina Dorsale: Materiali di partenza come piruvato, 3-fosfoglicerato o α-chetoglutarato vengono convertiti in scheletri carboniosi degli amminoacidi attraverso reazioni enzimatiche.
- Transaminazione: Un gruppo amminico viene trasferito da un amminoacido donatore (spesso il glutammato) a un acido α-cheto, formando il nuovo amminoacido.
- Riduzione e Modifica: Alcuni amminoacidi richiedono ulteriori passaggi enzimatici per raggiungere la loro struttura finale.
Enzimi e Cofattori Chiave
- Transaminasi (Aminotransferasi): Catalizzano il trasferimento del gruppo amminico.
- Glutammato Deidrogenasi: Coinvolta nella rimozione o aggiunta di gruppi amminici.
- Vitamina B6 (Piridossal Fosfato): Un cofattore essenziale per molte transaminasi.
Importanti Vie di Sintesi Specifiche
- Sintesi del Glutammato e della Glutammina: Il glutammato è un amminoacido centrale nel metabolismo dell'azoto. Viene sintetizzato dall'α-chetoglutarato e dall'ammoniaca tramite la glutammato deidrogenasi o la glutammina sintetasi. La glutammina viene formata aggiungendo un secondo gruppo amminico al glutammato.
- Sintesi della Serina: Deriva dal 3-fosfoglicerato, un intermedio della glicolisi, attraverso una serie di reazioni enzimatiche che includono idrossilazione, transaminazione e defosforilazione.
- Sintesi dell'Alanina: Principalmente ottenuta tramite la transaminazione del piruvato, utilizzando il glutammato come donatore di gruppi amminici.
- Sintesi della Tirosina: Avviene per idrossilazione della fenilalanina, un processo catalizzato dalla fenilalanina idrossilasi.
- Sintesi della Cisteina: La sintesi della cisteina coinvolge la serina e l'omocisteina, con l'enzima cistationina β-sintasi.
Gli amminoacidi aromatici (fenilalanina, tirosina, triptofano) derivano da fosfoenolpiruvato ed eritrosio-4-fosfato, attraverso la via dello shikimato che porta alla formazione del corismato, precursore comune.
La biosintesi degli amminoacidi non essenziali avviene principalmente in piante e microrganismi. Negli esseri umani, la maggior parte degli amminoacidi non essenziali può essere sintetizzata, mentre gli amminoacidi essenziali devono essere assunti con la dieta.
La sintesi degli amminoacidi è strettamente regolata da meccanismi come la regolazione allosterica e l'inibizione a feedback, che impediscono la sovrapproduzione e garantiscono un uso efficiente delle risorse metaboliche.
Disturbi nella sintesi degli amminoacidi possono portare a gravi patologie, come la fenilchetonuria (PKU), causata dall'incapacità di convertire la fenilalanina in tirosina, o l'omocistinuria, un difetto nel metabolismo della metionina.
Ruoli e Applicazioni degli Amminoacidi
Gli amminoacidi, oltre al loro ruolo fondamentale nella sintesi proteica, trovano applicazione in svariati settori industriali e hanno implicazioni significative per la salute umana.
Applicazioni Industriali
L'uso principale degli amminoacidi in campo industriale è come additivi nei mangimi per l'alimentazione animale. La metionina e la lisina, ad esempio, sono aggiunte per migliorarne il valore nutrizionale, consentendo agli animali di utilizzare meglio il cibo e produrre le proteine necessarie. Anche la treonina viene somministrata per alleviare infiammazioni intestinali e disturbi del metabolismo energetico.
In agricoltura, la capacità chelante degli amminoacidi viene sfruttata nei fertilizzanti per facilitare l'assorbimento di minerali da parte delle piante, correggendo carenze come la clorosi ferrosa. La metionina, inoltre, è impiegata come pesticida non tossico contro alcuni insetti.
L'industria farmaceutica utilizza alcuni amminoacidi o loro derivati. Il glutammato monosodico, sale dell'acido glutammico, è ampiamente utilizzato come esaltatore di sapidità in molti prodotti alimentari.
Amminoacidi e Salute Umana
Gli amminoacidi a catena ramificata (leucina, valina, isoleucina) possono avere effetti positivi sulle persone che praticano sport. Molti amminoacidi sono inclusi in integratori alimentari per supportare il sistema nervoso, migliorare il sonno e l'umore, rafforzare il sistema immunitario e contrastare problemi circolatori o digestivi.
Nell'industria cosmetica, gli amminoacidi proteici sono componenti importanti di prodotti per la cura della pelle, in particolare creme anti-età. Essi aiutano a rafforzare, idratare e rendere la pelle più elastica, reintegrando le carenze idriche e fungendo da precursori per la produzione di collagene.
Alcuni amminoacidi, come la taurina (un amminoacido non proteico), sono utilizzati negli integratori alimentari.
Produzione Commerciale
La produzione commerciale di amminoacidi si basa prevalentemente sulla fermentazione batterica, utilizzando batteri mutanti che producono in eccesso singoli amminoacidi a partire dal glucosio. La produzione annuale di glutammato, metionina e lisina rappresenta la quota maggiore della produzione globale di amminoacidi biogeni.
Metodi alternativi includono la sintesi chimica ed enzimatica, nonché conversioni enzimatiche di intermedi sintetici. In laboratorio, molti amminoacidi non proteinogenici vengono prodotti tramite sintesi di Strecker o amminazione riduttiva.
La ricerca attuale si concentra anche sulla sintesi di nuovi amminoacidi non naturali per la creazione di peptidomimetici, molecole con potenziali applicazioni biologiche e chimiche.
Il metabolismo degli amminoacidi
In sintesi, la biosintesi degli amminoacidi è un processo fondamentale che sostiene la vita, dalla costruzione delle proteine alla partecipazione a complesse vie metaboliche. La comprensione di questi percorsi è cruciale per la medicina, l'agricoltura e l'industria.
tags: #via #biosintetica #aminoacidica