Il triptofano, un amminoacido essenziale, riveste un ruolo cruciale in numerosi processi biochimici e fisiologici del nostro organismo. La sua scoperta nel 1901 da parte di Frederick Hopkins, attraverso l'idrolisi della caseina, segnò un punto di svolta nella comprensione della chimica delle proteine.
Origini e Isolamento
Frederick Hopkins, insieme a Sydney W. Cole, isolò per la prima volta il triptofano nel 1901. Questo avvenne tramite l'idrolisi della caseina, la principale proteina del latte. Il processo prevedeva la digestione della caseina in una soluzione di carbonato di sodio all'8%, seguita da una digestione triptica. Al termine di questo processo, l'amminoacido precipitato fu recuperato tramite filtrazione. Questo amminoacido, fondamentale per la vita, fu chiamato triptofano proprio in onore della tripsina utilizzata per la sua estrazione.
Caratteristiche Chimiche e Strutturali
Il triptofano è un amminoacido poco polare, caratterizzato da un gruppo laterale indolile. Questa struttura lo rende il precursore di una vasta gamma di composti, tra cui le triptamine. È una molecola chirale, il che significa che esiste in due forme speculari, ma solo l'isomero L è biologicamente attivo e utilizzato nella sintesi proteica. Inoltre, solo nella sua configurazione L, il triptofano è in grado di attraversare la barriera emato-encefalica, un aspetto fondamentale per la sua azione sul sistema nervoso centrale.
Produzione e Metabolismo
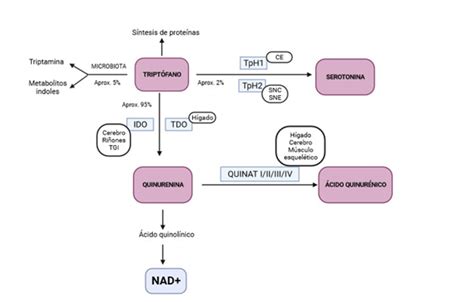
Oltre all'isolamento da fonti naturali, il triptofano viene prodotto industrialmente attraverso processi biotecnologici. La produzione biosintetica si basa sulla fermentazione di serina e indolo, utilizzando batteri come *Bacillus subtilis*, *Corynebacterium glutamicum*, *E. coli* e *Bacillus amyloliquefaciens*. Questi ceppi batterici sono geneticamente modificati per impedire la ricaptazione degli amminoacidi aromatici, ottimizzando così la produzione di triptofano. Una volta nell'organismo, il triptofano viene metabolizzato attraverso diverse vie, tra cui l'apertura dell'anello indolico con formazione di formilchinurenina e chinurenina. Il suo metabolismo è strettamente integrato con processi biochimici e fisiologici di grande importanza.
Ruolo Biologico e Applicazioni Terapeutiche
Il triptofano è il precursore di composti essenziali come la serotonina e la melatonina. La serotonina, un neurotrasmettitore, svolge un ruolo chiave nella regolazione dell'umore, dell'appetito, del sonno e della percezione del dolore. La melatonina, invece, è fondamentale per la regolazione dei ritmi sonno-veglia.
Per questo motivo, il triptofano è stato inizialmente distribuito come integratore alimentare e successivamente riconosciuto per la sua efficacia nel promuovere il sonno e nel contrastare i disturbi legati a bassi livelli di serotonina. Numerose ricerche cliniche hanno confermato la sua utilità come sonnifero naturale e come coadiuvante nel trattamento di disturbi dell'umore, mostrando particolare promessa come antidepressivo, sia da solo che in combinazione con altri farmaci.
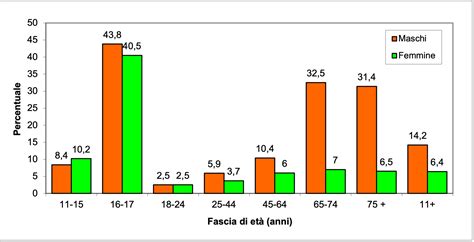
Il Triptofano e l'Emicrania
Studi recenti hanno evidenziato il coinvolgimento del triptofano nello sviluppo dell'emicrania. L'assunzione di triptofano si è dimostrata efficace nel migliorare la sintomatologia emicranica e nel ridurre il rischio di svilupparla. In particolare, un dosaggio di 1 g/die ha portato a una riduzione di circa il 60% del rischio di emicrania nella popolazione studiata. L'integrazione con triptofano, spesso associata ad altri nutrienti come magnesio, niacina e vitamina B6, rappresenta un approccio non farmacologico promettente nella gestione dell'emicrania.
Idrolisi della Caseina e Composizione Proteica
L'idrolisi della caseina, il processo attraverso cui il triptofano fu inizialmente isolato, è una tecnica utilizzata per scomporre le proteine nei loro amminoacidi costituenti. Questo processo può essere acido o enzimatico. L'idrolizzato di caseina viene impiegato per arricchire i cibi di proteine e come base per preparazioni proteiche liquide. È importante notare che durante l'idrolisi, soprattutto quella enzimatica, si possono verificare perdite di amminoacidi, con quelle di triptofano che sono particolarmente consistenti. Le proteine, fondamentali costituenti degli organismi viventi, sono polimeri complessi formati da amminoacidi legati tra loro. La loro composizione varia notevolmente, influenzando le proprietà specifiche di ciascuna proteina. Ad esempio, la gelatina non contiene triptofano, mentre la zeina ne è priva insieme a lisina e cisteina. Questa diversità nella composizione amminoacidica ha implicazioni significative, specialmente nell'alimentazione animale.
Reazioni Chimiche e Identificazione del Triptofano
Il triptofano partecipa a specifiche reazioni chimiche che ne permettono l'identificazione. La reazione di Hopkins e Cole, ad esempio, produce una colorazione rosso-violetta quando le sostanze proteiche contenenti triptofano vengono a contatto con una soluzione solforica di acido gliossilico. Questa reazione è distinta dalla reazione xantoproteica, data dalle proteine contenenti fenilalanina, tirosina o triptofano, che produce un colore giallo con acido nitrico concentrato. Un'altra reazione generale per proteine, peptoni e polipeptidi è la reazione del biureto.
Considerazioni sulla Sicurezza e sull'Integrazione
È fondamentale sottolineare che le informazioni presentate non costituiscono consiglio medico. L'uso del triptofano, soprattutto in dosi elevate, richiede cautela. Un episodio di epidemia di sindrome eosinofilo-mialgica negli Stati Uniti nel 1989, attribuito a un lotto di triptofano sintetizzato impropriamente, ha sollevato preoccupazioni sulla sicurezza. L'integrazione con triptofano può essere considerata sicura durante l'allattamento, ma nei soggetti "over 80" è consigliabile una somministrazione a dosi ridotte per evitare potenziali accumuli dovuti a un rallentamento metabolico. Per quanto riguarda l'emicrania, il dosaggio raccomandato per soggetti a rischio è di 1.000 mg prima di coricarsi, riducibile a 500 mg dopo un mese. Per disturbi dell'umore o del sonno, le modalità di assunzione possono variare, spesso in associazione con altri nutrienti o farmaci, e richiedono un'attenta valutazione medica.
Il neurotrasmettitore della serotonina spiegato in 5 minuti | Percorso 5-HT | SSRI
tags: #hopkins #idrolisi #caseina #triptofano