La fosfatidil inositolo 3 chinasi (PI3K) è una famiglia di enzimi intracellulari che svolgono un ruolo fondamentale nella segnalazione cellulare. Questi enzimi sono così chiamati per la loro capacità di fosforilare la posizione idrossilica D-3 dell'anello inositolo del fosfatidil inositolo (PtdIns) e dei suoi derivati fosforilati, PtdIns(4)P e PtdIns(4,5)P2.
La funzione della fosfatidil inositolo 3 chinasi è centrale nella regolazione di molti processi cellulari fondamentali. Dopo l'attivazione, la PI3K genera PIP3, che recluta e attiva una varietà di proteine effettrici a valle contenenti domini pleckstrin omologia (PH), come Akt (nota anche come Proteina Chinasi B) e la fosfoinositide-dipendente chinasi 1 (PDK1).
Il ruolo della fosfatidil inositolo 3 chinasi si estende a una vasta gamma di attività cellulari, influenzando la crescita, la divisione, la sopravvivenza e l'interazione delle cellule con il loro ambiente.
Le PI3K sono ampiamente classificate in tre classi (Classe I, II e III) in base alla loro struttura, specificità del substrato e meccanismi regolatori. Le PI3K di Classe I sono le più studiate, in particolare per il loro coinvolgimento nella crescita cellulare, nella sopravvivenza e nella proliferazione, e per la loro frequente disregolazione nelle malattie umane.
Classi di Fosfatidil Inositolo 3 Chinasi
Le PI3K sono ampiamente categorizzate in tre classi (Classe I, II e III) basate sulla loro struttura, specificità del substrato e meccanismi regolatori.
Classe I
Le PI3K di Classe I sono le più studiate, in particolare a causa del loro coinvolgimento nella crescita cellulare, nella sopravvivenza e nella proliferazione, e della loro frequente disregolazione nelle malattie umane. Le PI3K di Classe I catalizzano la conversione del fosfatidil inositolo (4,5)-bisfosfato (PI(4,5)P2) in fosfatidil inositolo (3,4,5)-trifosfato (PI(3,4,5)P3) in vivo. Le PI3K di Classe I sono molecole eterodimeriche composte da una subunità regolatoria e una catalitica; sono ulteriormente suddivise nei sottoinsiemi IA e IB in base alla somiglianza delle sequenze.
Le PI3K di Classe IA sono composte da un eterodimero tra una subunità catalitica p110 e una subunità regolatoria più corta (spesso p85). Esistono cinque varianti della subunità regolatoria: le tre varianti di splicing p85α, p55α e p50α, p85β e p55γ. Esistono anche tre varianti della subunità catalitica p110 designate come subunità catalitica p110α, β o δ. Le prime tre subunità regolatorie sono tutte varianti di splicing dello stesso gene (Pik3r1), mentre le altre due sono espresse da altri geni (Pik3r2 e Pik3r3, rispettivamente p85β e p55γ). La subunità regolatoria più espressa è p85α; tutte e tre le subunità catalitiche sono espresse da geni separati (Pik3ca, Pik3cb e Pik3cd per p110α, p110β e p110δ, rispettivamente). Le prime due isoforme di p110 (α e β) sono espresse in tutte le cellule, ma p110δ è espresso principalmente nei leucociti, e si suggerisce che si sia evoluto parallelamente al sistema immunitario adattativo. Le subunità p85 contengono domini SH2 e SH3.
Classe II
Le PI3K di Classe II e III si differenziano dalla Classe I per struttura e funzione. La caratteristica distintiva delle PI3K di Classe II è il dominio C2 C-terminale. La Classe II comprende tre isoforme catalitiche (C2α, C2β e C2γ), ma, a differenza delle Classi I e III, non presenta proteine regolatrici. La Classe II catalizza la produzione di PI(3)P da PI e PI(3,4)P2 da PI(4)P; tuttavia, si sa poco sul loro ruolo nelle cellule immunitarie.
Classe III
Le PI3K di Classe III producono solo PI(3)P da PI, ma sono più simili alla Classe I per struttura, in quanto esistono come eterodimeri di una subunità catalitica (Vps34) e una regolatoria (Vps15/p150). La Classe III sembra essere principalmente coinvolta nel traffico di proteine e vescicole.
Ruolo delle PI3K nella Segnalazione Cellulare
Le PI3K sono coinvolte in una gamma straordinariamente diversificata di funzioni cellulari, tra cui la crescita cellulare, la proliferazione, la differenziazione, la motilità, la sopravvivenza e il traffico intracellulare. Molte di queste funzioni sono correlate alla capacità delle PI3K di Classe I di attivare la proteina chinasi B (PKB, nota anche come Akt) come nel percorso PI3K/AKT/mTOR.
Le isoforme p110δ e p110γ regolano diversi aspetti delle risposte immunitarie. Le PI3K sono anche un componente chiave del percorso di segnalazione dell'insulina. Pertanto, vi è un grande interesse nel ruolo della segnalazione PI3K nel diabete mellito.
Il dominio pleckstrin omologia di AKT si lega direttamente a PtdIns(3,4,5)P3 e PtdIns(3,4)P2, che sono prodotti dalle PI3K attivate. Poiché PtdIns(3,4,5)P3 e PtdIns(3,4)P2 sono confinati alla membrana plasmatica, ciò si traduce nella traslocazione di AKT alla membrana plasmatica. Allo stesso modo, la fosfoinositide-dipendente chinasi-1 (PDK1 o, raramente indicata come PDPK1) contiene anch'essa un dominio pleckstrin omologia che si lega direttamente a PtdIns(3,4,5)P3 e PtdIns(3,4)P2, causandone anch'essa la traslocazione alla membrana plasmatica dopo l'attivazione della PI3K. L'interazione tra PDK1 attivata e AKT consente ad AKT di essere fosforilato da PDK1 sulla treonina 308, portando alla parziale attivazione di AKT.
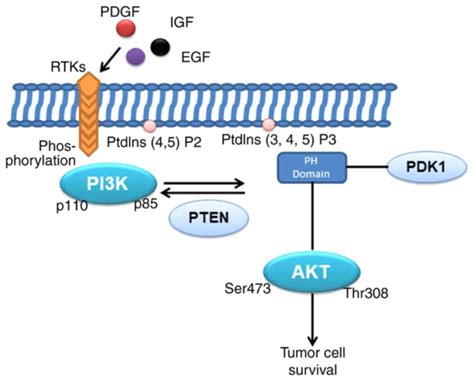
Il percorso PI3K/AKT si è dimostrato necessario per una gamma estremamente diversificata di attività cellulari, in particolare la proliferazione e la sopravvivenza cellulare.
Le PI3K e il Cancro
La PI3K di Classe IA p110α è mutata in molti tumori. Molte di queste mutazioni rendono la chinasi più attiva. È la chinasi più frequentemente mutata nel glioblastoma, il tumore cerebrale primario più maligno. La fosfatidil inositolo (3,4,5)-trifosfato fosfatasi PTEN, che antagonizza la segnalazione PI3K, è assente in molti tumori. Inoltre, il recettore del fattore di crescita epidermico EGFR, che funziona a monte della PI3K, è mutazionalmente attivato o sovraespresso nel cancro. Pertanto, l'attività della PI3K contribuisce in modo significativo alla trasformazione cellulare e allo sviluppo del cancro.

Le PI3K e la Plasticità Sinaptica
Le PI3K sono state anche implicate nella potenziamento a lungo termine (LTP). Se siano necessarie per l'espressione o l'induzione dell'LTP è ancora dibattuto. Nei neuroni CA1 dell'ippocampo di topo, determinate PI3K sono complesse con i recettori AMPA e compartimentalizzate nella densità postsinaptica delle sinapsi glutamatergiche. Le PI3K vengono fosforilate in seguito all'attività della CaMKII dipendente dal recettore NMDA, e ciò facilita l'inserimento delle subunità GluR1 dei recettori AMPA nella membrana plasmatica. Ciò suggerisce che le PI3K siano necessarie per l'espressione dell'LTP.
Inibitori delle PI3K
Tutte le PI3K sono inibite dai farmaci wortmannin e LY294002, sebbene alcuni membri della famiglia delle PI3K di Classe II mostrino una ridotta sensibilità. Poiché wortmannin e LY294002 sono inibitori ad ampio spettro delle PI3K e di numerose proteine non correlate a concentrazioni più elevate, sono troppo tossici per essere utilizzati come terapie. Pertanto, numerose aziende farmaceutiche hanno sviluppato inibitori specifici per le isoforme di PI3K. A gennaio 2019, tre inibitori di PI3K sono approvati dalla FDA per l'uso clinico di routine nell'uomo: l'inibitore di PIK3CD idelalisib (luglio 2014), l'inibitore duale PIK3CA e PIK3CD copanlisib (settembre 2017) e l'inibitore duale PIK3CD e PIK3CG duvelisib (settembre 2018).
Percorso PI3K AKT mTOR (e gli effetti)
| Variante | Descrizione |
|---|---|
| Variante 1 | Rappresenta il trascritto più lungo. |
| Variante 2 | Differisce nella regione 5' UTR rispetto alla variante 1. |
| Variante 4 | Contiene un esone alternativo e utilizza un sito di splicing alternativo nella regione codificante 5'. Queste differenze causano l'inizio della traduzione a un codone di inizio a monte rispetto alla variante 1. |
| Variante 5 | Manca un esone alternativo in-frame nella regione codificante centrale rispetto alla variante 1. |
| Variante 6 | Differisce nella regione 5' UTR e nella sequenza codificante rispetto alla variante 1. L'isoforma risultante (5) è più corta all'N-terminus rispetto all'isoforma 1. |
| Variante 7 | Differisce nella regione 5' UTR e nella sequenza codificante rispetto alla variante 1. L'isoforma risultante (5) è più corta all'N-terminus rispetto all'isoforma 1. |
| Variante 8 | Differisce nella regione 5' UTR e nella sequenza codificante rispetto alla variante 1. L'isoforma risultante (5) è più corta all'N-terminus rispetto all'isoforma 1. |
| Variante 9 | Differisce nella regione 5' UTR e nella sequenza codificante rispetto alla variante 1. L'isoforma risultante (5) è più corta all'N-terminus rispetto all'isoforma 1. |
| Variante 10 | Manca un esone alternativo in-frame all'estremità 3' rispetto alla variante 1. |
| Variante 11 | Manca un esone alternativo all'estremità 5' e utilizza un codone di inizio a valle rispetto alla variante 1. |
| Variante 12 | Manca due esoni alternativi all'estremità 5' e utilizza un codone di inizio a valle rispetto alla variante 1. |
| Variante 14 | Manca un esone alternativo rispetto alla variante 1. |
tags: #fosfatidil #inositolo #3 #kinasi