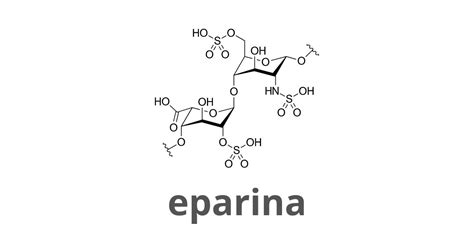
L’eparina, il cui nome deriva dal greco "ἧπαρ" (fegato), è stata originariamente estratta dal fegato di cane. Si tratta di un polisaccaride altamente solfatato appartenente alla famiglia dei glicosaminoglicani (GAG). Questi ultimi sono catene non ramificate composte da unità di disaccaridi ripetute, in cui uno degli zuccheri è un amminozucchero (N-acetilglucosammina o N-acetilgalattosammina) e l’altro è un acido glucuronico o iduronico. I GAG contengono gruppi solforici o carbossilici che conferiscono loro un'elevata carica negativa, caratteristica che si ritrova anche nell'eparina, la quale possiede la più alta densità di carica negativa tra tutte le biomolecole conosciute.
L'eparina è un carboidrato con un intervallo di peso molecolare che varia da 3.000 a 30.000 Da, sebbene le eparine commerciali abbiano un peso molecolare medio compreso tra 12 e 15 KDa. In natura, l'eparina è un polimero con una catena di varie dimensioni. Per rendere la sua farmacodinamica più prevedibile, sono state sviluppate le eparine a basso peso molecolare (LMWH), che subiscono un processo di frazionamento.
La più comune unità disaccaridica che compone l'eparina è costituita da acido iduronico 2-solfato e 6-O-solfato, glucosamina N-solfato (IdoA(2S)-GlcNS(6S)). In minore misura, si possono trovare disaccaridi contenenti glucosamina 3-O-solfato o glucosamina con un gruppo amminico libero.
L'eparina svolge un ruolo cruciale nella regolazione della coagulazione del sangue grazie al suo legame con diverse proteine, in particolare con l'antitrombina (AT), una proteina prodotta dal fegato. Questo legame provoca un cambiamento conformazionale nell'antitrombina, esponendo il suo sito attivo. L'antitrombina attivata inattiva la trombina (Fattore IIa), il Fattore X, e altre proteasi coinvolte nella cascata coagulativa.
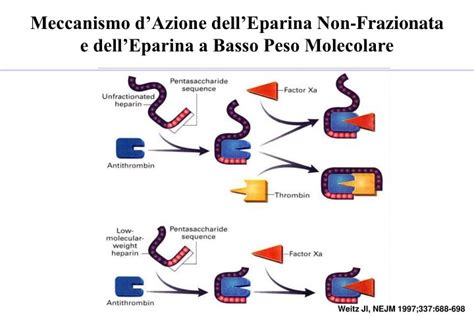
In particolare, il legame tra eparina e antitrombina permette la disattivazione del Fattore Xa. Affinché ciò avvenga, è necessario un legame tra la sequenza pentasaccaridica dell'eparina e il Fattore Xa stesso. La formazione di un complesso ternario tra AT-III, trombina ed eparina porta all'inattivazione della trombina. È importante notare che le molecole di eparina con meno di 18 saccaridi non possiedono la lunghezza di catena necessaria per fare da ponte tra trombina e AT, quindi non sono in grado di inibire la trombina. Al contrario, frammenti molto piccoli contenenti la sequenza pentasaccaridica sono in grado di inibire il Fattore Xa tramite l'AT.
In dosi terapeutiche, l'eparina agisce come anticoagulante, prevenendo la formazione di coaguli e l'estensione di quelli già esistenti. Non rompe direttamente i trombi già formati, ma facilita l'azione dei meccanismi di lisi del trombo per abbatterli. L'eparina è efficace per la prevenzione di trombi murali dopo infarto del miocardio e viene utilizzata per trattare e prevenire la trombosi venosa profonda, l'embolia polmonare e la tromboembolia arteriosa. È altresì impiegata nel trattamento di attacchi cardiaci e angina instabile.
L'eparina viene somministrata per via parenterale (endovenosa o sottocutanea) poiché non viene assorbita dall'intestino a causa della sua elevata carica negativa e delle dimensioni molecolari. Le iniezioni intramuscolari vengono evitate per il rischio di formazione di ematomi. L'uso di LMWH ha reso possibile il dosaggio una volta al giorno, eliminando la necessità di un'infusione continua.
La scoperta dell'eparina risale al 1916, grazie a Jay McLean e William Henry Howell, anche se gli studi clinici iniziarono solo nel 1935. Negli anni '30, i Connaught Medical Research Laboratories perfezionarono una tecnica di produzione sicura ed efficace.
La tecnica per autosomministrare l'eparina
Un grave effetto collaterale dell'eparina è la trombocitopenia indotta da eparina (HIT), una reazione immunologica che porta alla degradazione delle piastrine. Questa condizione può essere evitata con l'uso di eparine sintetiche. Altri effetti collaterali includono l'aumento dei livelli di aminotransferasi sierica e l'iperkaliemia (soppressione dell'aldosterone indotta da eparina).
Per contrastare questi effetti o per pazienti con HIT, sono stati sviluppati anticoagulanti farmaceutici come le eparine a basso peso molecolare (LMWH) e il Fondaparinux. Questi farmaci mirano all'attività antifattore Xa, consentendo una regolazione più sottile della coagulazione e un indice terapeutico migliorato, riducendo il rischio di osteoporosi e HIT. Il Danaparoid, una miscela di eparan solfato, dermatan solfato e condroitin solfato, può essere utilizzato come anticoagulante in pazienti con HIT.
Gli effetti dell'eparina vengono monitorati in laboratorio tramite il tempo parziale di tromboplastina (aPTT). L'eparina può essere utilizzata come terapia anticoagulante iniziale, in attesa di un anticoagulante orale per terapie a lungo termine.
Oltre all'uso farmaceutico come anticoagulante, l'eparina può essere impiegata come collirio o per creare superfici anticoagulanti in esperimenti e cure mediche, come l'emodialisi.
I glicosaminoglicani (GAG), come l'eparina, si trovano in vivo legati covalentemente a proteine, formando strutture complesse note come proteoglicani. Svolgono ruoli essenziali nelle matrici tissutali, fornendo proprietà lubrificanti, protettive e connettive. La loro capacità di formare gel porosi e idratati è fondamentale per la matrice extracellulare, facilitando la diffusione di molecole idrosolubili e la migrazione cellulare, oltre a conferire resistenza alle forze di compressione.

tags: #eparina #glucosamino #glicano